تجزیه عنصری ، تفکیک مخلوط ترکیبات آلی
تجزیه عنصری ، تفکیک مخلوط ترکیبات آلی
تفکیک مخلوط تر کیبات آلی:
در شناسایی ترکیبات آلی شیمیدان کمتر به یک جسم خالص برخورد می کند بلکه اکثرا جسم با محصولات فرعی و مواد اولیه مخلوط است.گرچه با وجود روش های جدید تفکیک بخصوص روشهای کروماتوگرافی جدا کردن ترکیب خالص از گذشته آسانتر است با این حال نباید اهمیت روشهای کلاسیک را نادیده گرفت.
اساس کلی روشهای که اغلب برای جدا کردن مخلوط های آلی به کارمی رود استفاده از قطبیتی است که در اجزای یک مخلوط وجود دارد یا در آن ایجاد می شود.این اختلاف تقریبا در تمام روشهای تفکیک از جمله تقطیر –تبلور مجدد-استخراج و کروماتوگرافی به کار می آید.بزرگترین قطبیتی که تفکیک را ساده تر می کند اختلافی است که در قطیبت نمکها و مواد آلی غیر قطبی وجود دارد.هر گاه یک یا چند جزاز یک مخلوط قابل تفکیک به نمکهای مربوط باشند به سهولت می توان آن اجزا را به کمک استخراج یا تقطیر به طور کامل از اجزای غیر قطبی جدا کرد.
تجزیه کیفی آلی به روش کلاسیک:
این تجزیه شامل ۶ مرحله ی اساسی است که در زیر آرده شده است:
۱)آزمایش مقدماتی خواص فیزیکی و شیمیایی
۲)اندازه گیری ثابت های فیزیکی
۳)تجزیه عنصری
۴)آزمایشهای مربوط به حلالیت
۵)آزمایشهای مربوط به گروه بندی(فعالیت عوامل مختلف غیر از واکنشهای اسیدو باز)
۶)تهیه مشتق ها
این روش بسیار با ارزش است.با این روش معمولا می توان یک ترکیب آلی شناخته شده را نسبت به یک ترکیب معدنی با اطمینان بیشتری تشخیص داد.
در ادامه به شرح مورد سوم(تجزیه عنصری) می پردازیم.

تجزیه عنصری
عنا صر متداول موجود درترکیبات آلی کربن هیدروژن واکسیژن می باشد گاهی عناصر دیگری نظیر نیتروژن- گوگرد-اکسیژن و هالوژن هاهم درآنها یافت می شوند .
برای اکسیژن آزمایش ساده ای وجود نداردو عناصر دیگر با پیوند کوالانسی در اتصال هستندو بنابراین با آزمایش های یونی معمولی مستقیما جواب نمی دهند.ولی اگر جسم آلی مجهول با سدیم مذاب ذوب شود در اگثر موارد طوری ترکیب می شود که NوSوXآن به یونهای CNوSوCNSوXتبدیل می شود.پس از آنکه سدیم اضافی دقیقا از بین برده شد محلول آبی را که محتوی این یونهاست به روش معمولی معدنی تجزیه می کنند.توضیح کامل تری در این مورد وجود دارد که در زیر به آن می پردازیم.
کربن هیدروژن واکسیژن
برای اثبات وجود کربن و هیدروژن نمونه رابا پودر خشک مس(II) اکسید حرارت داده که منجر به ایجاد کربن دی اکسید وآب می شود . حضور کربن در نمونه با عبور دادن گاز های ایجاد شده از درون محلول با ریم یا کلسیم هیدروکسید مشخص نمی شود که دراین صورت رسوب کربنات مربوطه حاصل می شود . هیدروژن را می توان با ایجاد قطره های آب متراکم شده روی قسمت بالایی لوله تشخیص داد . هیچ آزمایش کیفی برای اثبات وجود اکسیژن در ترکیبات آلی وجود ندارد برای تعیین اکسیژن باید تجزیه کمی صورت بگیرد .دراین روش اگر اگر مجموع درصد تمام عناصر تشکیل دهنده ترکیب کمتر آن تا ۱۰۰ مربوط به در صداکسیژن است .
نیتروژن گوگرد و هالوژن ها
تشخیص کیفی این عناصر در ترکیبات آلی مشکل تراز آنها در ترکیبات معدنی است . زیرا اکثر ترکیبات آلی در حالت محلول درآب به مقدار قابل ملاحظه ای یونیزه نمی گردند.از آنجا که آزمایشهای تجزیه کیفی براساس واکنش های یونی می باشند انها را نمی توان مستقیما برای ترکیبات آلی به کار گرفت.به عنوان مثال سدیم کلرید یا سدیم برمید با محلول آبی نقره نیترات به مقدار قابل توجهی رسوب هالید های نقره را ایجاد می نمایند در حالیکه کربن تترا کلرید –برومو بنزن و اغلب هالیدهای آلی در هنگام واکنش با محلول آبی نقره نیرات رسوب هالید نقره را ایجاد نمی نمایند زیرا در آنها به میزان یون هالید در محلول تولید نمی شود.
در این حالت برای تشخیص کیفی لازم است که ابتدا عناصر نیتروژن-گوگرد-و هالوژن ها را به ترکیبات یونیزه شونده تبدیل نمود.یکی از متداول ترین این روش هاجهت انجام این تبدیل ذوب کردن نمونه با فلز سدیم است که با انجام آن عناصر ذکر شده به ترکیبات سدیم سیانید-سدیم سولفیدو سدیم هالید تبدیل می شوند.سپس آنیون های حاصل را می توان توسط آزمایش های معمول معدنی شناسایی نمود.
واکنش ذوب با سدیم به صورت زیر می باشد:
در مواردی که سدیم به مقدار کافی به کار برده نشود و ماده مورد نظر دارای گوگرد ونیتروژن (هردو)باشد گاهی تفکیک به خوبی صورت نمی گیرد واین دو عنصر به صورت ترکیب NaSCNظاهر می گردند.برای شناسایی این ترکیب از کلرو فرمیک۱۰درصد استفاده می شود.
تجزیه کیفی مواد آلی به روش ذوب قلیایی جهت تشخیص نیتروژن، گوگرد و هالوژنها
برای تشخیص این عناصر در ترکیبات آلی ابتدا باید آنها را به ترکیبات معدنی یونیزه تبدیل کرد سپس شناسایی نمود. این تبدیل ممکن است به روشهای مختلف صورت گیرد ولی بهترین روش ذوب ترکیبات با فلز سدیم است. در این روش سیانید سدیم (NaCN)، سولفید سدیم (Na2S) و هالید سدیم (NaX) تشکیل میشود که به آسانی قابل تشخیص هستند.
معمولا سدیم به مقدار اضافی به کار برده میشود. در غیر اینصورت اگر گوگرد و نیتروژن هردو وجود داشته باشند. احتمالا تیوسیانات سدیم (NaSCN) تشکیل میشود. در این صورت در تشخیص نیتروژن به جای آبی پروس رنگ قرمز مشاهده میشود زیرا بجای یون (CN-)، یون (SCN-) خواهیم داشت. اما با سدیم اضافی تیوسیانات تشکیل شده تجزیه میشود و جواب درست به دست می آید.
مخلوط حاصل آب اضافه کرده مخلوط قلیایی را صاف نموده و سپس به آن (FeSO4) اضافه کنید در این صورت فروسیانید سدیم تشکیل میشود.
وقتی محلولهای قلیایی نمکهای فروی بالا جوشانده میشود بر اثر اکسیژن هوا کمی یون فریک تشکیل میشود. (بر اثر سولفوریک اسید رقیق هیدروکسیدهای فرو و فریک تشکیل شده حل میشوند) فروسیانیدها با نمک فریک تشکیل فروسیانید فریک (آبی پروس) میدهند.
برای اسیدی کردن محیط نباید از (HCl) استفاده کرد زیرا به علت تشکیل (FeCl6) رنگ زرد در محیط ایجاد میشود و به جای آبی پروس رنگ سبز ظاهر میشود. به همین دلیل کلرید فریک نیز نباید اضافه شود. همانطوری که قبلا ذکر شده است بر اثر اکسیداسیون به وسیله هوا در محیطهای قلیایی گرم به مقدار کافی یونهای فریک تشکیل میشود بنابراین نیازی به افزایش یون فریک نیست، افزایش مقدار کمی محلول رقیق فلوئورید پتاسیم ممکن است به تشکیل آبی پروس در محلول که به آسانی قابل صاف شدن است کمک نماید (Fe3+ با F- تولید FeF63- میکند که پایدار است و باعث خارج شدن Fe3+ از محیط عمل میشود).
گوگرد به صورت یون سولفید را میتوان به وسیله استات سرب و استیک اسید و یا به وسیله پلمبیت سدیم (محلول قلیایی استات سرب) به صورت رسوب سولفید سرب (PbS) سیاه رنگ تشخیص داد.
برای تشخیص یونهای هالوژن (Cl, Br, I) از اثر محلول نیترات نقره در محیط اسید نیتریکی استفاده میشود در این صورت هالید نقره به صورت رسوب حاصل میشود.
بخش عملی (ذوب قلیایی)
احتیاط: (به هنگام کار عینک محافظ فراموش نشود) در یک لوله آزمایش کاملا خشک (حدود ۱۵۰ در ۱۲ میلیمتر غیر پیرکس) یک تکه سدیم کوچک تمیز به ابعاد تقریبی ۴ میلیمتر بیندازید (سدیم را به وسیله کاردک تمیز و خشک بردارید) و لوله را با گیره بگیرید و ته لوله را با شعله کوتاه به ملایمت حرارت دهید تا سدیم در داخل لوله ذوب شده و به صورت دود سفید در آید و بخارات تا ارتفاع حدود ۲ سانتی متر بالا رود، سپس لوله را از شعله دور کرده و به آن چند ذره جسم جامد (حدود ۲۰ میلی گرم) یا حدود سه قطره مایع مورد آزمایش (ترجیحا طی چند نوبت) طوری اضافه کنید که مستقیما در ته لوله و بر روی دود سفید سدیم ریخته شود (دقت کنید ممکن است انفجار کوچکی رخ دهد بنابر این این آزمایش را حتما زیر هود و تحت نظر مربی آزمایشگاه انجام دهید) و بعد بتدریج لوله را تا سرخ شدن گرم کنید (احتیاط: موقع حرارت دادن، دهانه لوله را به طرف خود یا فرد دیگری نگیرید) سپس لوله داغ را داخل یک بشر کوچک حاوی ۱۰ میلی لیتر آب مقطر وارد کنید تا بشکند. مخلوط را تا جوش حرارت داده و سپس صاف کنید محلول صاف شده باید زلال و قلیایی باشد. در صورتیکه تیره باشد، احتمالا تجزیه ناقص بوده و ذوب قلیایی باید دوباره تکرار شود.
روش دیگر استفاده از لوله آزمایش پیرکس است. در این روش مطابق بالا عمل کنید اما پس از ذوب قلیایی اجازه دهید لوله سرد شود و سپس ۳ الی ۴ میلی لیتر متانول به آن اضافه کنید تا سدیم اضافی را تجزیه کند سپس بر روی آن آب مقطر بریزید تا نصف لوله پر شود و برای چند دقیقه به ملایمت بجوشانید. سپس مخلوط را صاف نموده و بر روی محلول آزمایشات زیر را انجام دهید.
شناسایی نیتروژن
حدود ۱ میلی لیتر محلول صاف شده را در یک لوله آزمایش ریخته و به آن کمی سولفات فرو اضافه کنید و محلول را به آرامی و همراه با تکان دادن تا نقطه جوش حرارت دهید و سپس بدون سرد نمودن محلول را با اسید سولفوریک رقیق اسیدی کنید(PH=13) رسوب یا رنگ آبی پروس دلیل بر وجود نیتروژن است. افزودن ۱ میلی لیتر محلول ۵% فلوئورید پتاسیم برای تشکیل آبی پروس مفید است.
شناسایی گوگرد
الف) استفاده از استات سرب: در حدود ۱ میلی لیتر محلول زیر صافی را در یک لوله آزمایش ریخته و با استیک اسید اسیدی کنید. حال به محلول حاصل چند قطره استات سرب اضافه کنید. ایجاد رسوب سیاه رنگ سولفید سرب دلیل بر وجود گوگرد در ماده آلی است.
ب) استفاده از پلمبیت سدیم: ابتدا محلول پلمبیت سدیم را به این صورت تهیه کنید. به چند قطره محلول استات یا نیترات سرب قطره قطره محلول سود ۱۰% اضافه کنید تا ابتدا رسوب سفید تشکیل شده سپس در زیادی سود حل شود و محلول زلالی به دست آید. در حدود ۱ میلی لیتر محلول زیر صافی را در یک لوله آزمایش ریخته و حدود یک میلی لیتر محلول پلمبیت سدیم به آن اضافه کنید. تشکیل رسوب سیاه رنگ PbS نشانه وجود گوگرد در جسم مورد آزمایش است.
شناسایی هالوژنها
آزمایش نیترات نقره
اگر در ساختمان ماده آلی نیتروژن یا گوگرد حضور داشته باشد با افزایش نیترات نقره به محلول اسیدی تهیه شده از ذوب قلیایی علاوه بر هالید نقره، رسوب سفید AgCN یا رسوب Ag2S نیز تشکیل میشود که مزاحم عمل تشخیص هالوژنها هستند بنابراین قبل از رسوب دادن AgX باید گوگرد و نیتروژن را از محیط عمل خارج سازید، بدین طریق که به آن اسید نیتریک غلیظ افزوده و محلول حاصل را بجوشانید تا بر اثر تبخیر حجم آن به نصف تقلیل داده شود، سپس آنرا سرد کرده و با حجم مساوی آب مقطر رقیق کنید. سپس بر روی آن آزمایشات زیر را انجام دهید، اگر گوگرد و ازت وجود نداشته باشد نیازی به عمل فوق نیست.
الف) اگر در جسم آلی یک نوع هالوژن وجود داشته باشد حدود ۲ میلی لیتر از محلول زیر صافی را در یک لوله آزمایش بریزید و با اسید نیتریک رقیق آنرا اسیدی کرده مقداری محلول نیترات نقره اضافه کنید، رسوب تشکیل شده مشخص کننده نوع هالوژن خواهد بود، مایع رویی را بر اثر سرازیر کردن جدا کنید و به رسوب محلول رقیق آمونیاک اضافه نمائید اگر رسوب سفید بوده و به خوبی محلول در آمونیاک رقیق باشد نشانه کلر، و اگر زرد کمرنگ و به سختی محلول در آمونیاک باشد (کم محلول باشد) نشانه برم، اگر زرد پر رنگ و تقریبا نا محلول در آمونیاک باشد نشانه وجود ید در جسم آلی است.
ب) اگر مخلوط چند هالوژن وجود داشته باشد:
شناسایی ید
۲ میلی لیتر از محلول زیر صافی را در یک لوله آزماش بریزید و با مقداری استیک اسید خالص (گلاسیال)، آنرا اسیدی کنید و سپس به آن حدود یک میلی لیتر تتراکلرید کربن بیفزائید و قطره قطره محلول نیتریت سدیم ضمن تکان دادن شدید لوله آزمایش اضافه کنید رنگ بنفش یا ارغوانی که در لایه آلی (CCl4) تشکیل میشود نشانه حضور ید است.
پس از تشخیص ید از محلول همین لوله آزمایش برای تشخیص برم استفاده کنید. بدین طریق که مجددا مقداری محلول نیتریت سدیم افزوده و مقدار جزئی گرم کنید. بعد شدیدا تکان دهید و صبر کنید تا دو لایه از هم جدا شوند، لایه رویی را در لوله آزمایش تمیز دیگری بریزید و لایه بنفش رنگ تتراکلرید کربن را دور بریزید. به لایه رویی که در لوله آزمایش تمیز ریخته بودید یک میلی لیتر تترا کلرید کربن اضافه کنید و قطره قطره محلول ۲۰% نیتریت سدیم بیفزائید و در ضمن افزایش لوله را تکان دهید اگر باز هم لایه زیری رنگی شد محلول سدیم نیتریت بیشتری ریخته و پس از تکان دادن و سپس جدا شدن دو لایه لایه رویی را به لوله آزمایش دیگری منتقل کنید و لایه زیری را دور بریزید و بر روی لایه رویی این عمل را آنقدر تکرار کنید تا دیگر لایه رنگی ایجاد نشود، در این صورت دیگر در محلول شما ید وجود ندارد. حال بر روی این محلول آزمایش تشخیص برم انجام دهید. (توجه کنید که اگر در ابتدای آزمایش رنگ بنفش ظاهر نشود نشانه عدم حضور ید در محلول است و بنابر این نیازی به استخراج ید نیست و از همان ابتدا میتوان برای تشخیص برم عمل کرد).
شناسایی برم
محلول اسیدی فوق را زیر هود حرارت دهید تا دیگر بخارات NO خارج نشود، سپس سرد کنید. محلول را با استیک اسید گلاسیال به شدت اسیدی کرده و مقدار کمی از دی اکسید سرب PbO2 اضافه نمائید. یک تکه کاغذ صافی آغشته به محلول فلورسئین را در بالای دهانه لوله آزمایش به دور دهانه چسبانده و حرارت دهید (کاغذ آغشته به فلورسئین به رنگ زرد لیمویی است) دی اکسید سرب در محلول استیک اسید تولید استات سرب میکند که HBr و HI را اکسید میکند ولی عملا تحت شرایط فوق بر HCl اثری ندارد.
(۱) ائوسین (قرمز رنگ) و (۲) فلوئورسئین (زردرنگ)
چون در داخل لوله آزمایش ید وجود ندارد اگر کاغذ آزمایش فلورسئین به رنگ صورتی در آید نشانه وجود برم در جسم آلی است (البته باید توجه داشت که ید نیز چنین جوابی میدهد بنابر این باید ابتدا ید را کاملا از محیط عمل خارج ساخت و سپس آزمایش مربوط به برم را انجام داد) برای تشخیص کلر از محتویات همین لوله استفاده میکنیم
شناسایی کلر
اگر در آزمایش بالا کاغذ آزمایش فلورسئین به رنگ صورتی در نیاید دلیل آن است که در جسم مورد نظر برم شرکت ندارد در این صورت لوله آزمایش را با کمی آب مقطر بشوئید و محلول حاصل را صاف کنید و به محلول زیر صافی محلول رقیق اسید نیتریک و نیترات نقره اضافه کنید تشکیل رسوب سفید کلوئیدی نشانه وجود کلر است اما اگر در آزمایش قبل کاغذ آزمایش فلورسئین به رنگ صورتی در آید، عمل حرارت دادن را آنقدر ادامه دهید تا دیگر کاغذ آزمایش فلورسئین را به رنگ صورتی در نیاورد (در صورت لزوم مجددا کمی PbO و CH3COOH اضافه کنید) البته این آزمایش را میتوان بر محلول اولیه حاصل شده از ذوب قلیایی نیز انجام داد که در این صورت برم و ید هردو از محیط عمل خارج میشوند در این حالت حرارت را قطع کنید. پس از سرد شدن محلول محتویات آنرا با کمی آب مقطر بشوئید و صاف کنید و به محلول زیر صافی محلول رقیق اسید نیتریک و نیترات نقره اضافه کنید تشکیل رسوب سفید نشانه وجود کلر در جسم آلی است در اینجا برای انحلال این رسوب سفید نمیتوان از آمونیاک استفاده کرد، و اگر به محلول کلوئیدی فوق آمونیاک اضافه کنید مقدار رسوب سفید زیادتر خواهد شد. چرا؟ (یاد آوری: اگر ید و برم قبلا بطور کامل خارج نشده باشند، مقدار جزئی آنها نیز رسوب تقریبا سفید ایجاد خواهد کرد که با رسوب سفید کلرید نقره قابل اشتباه خواهد بود)
روش تشخیص هالوژنها با استفاده از آب کلر
اگر مخلوطی از هالوژنها داشته باشید برای تشخیص هر یک از آنها با آب کلر مطابق زیر عمل کنید:
مقدار ۲-۱ میلی لیتر از محلول زیر صافی حاصل از ذوب قلیایی را به وسیله اسید کلریدریک رقیق اسیدی کنید و یک میلی لیتر تتراکلرید کربن و سپس یک قطره آب کلر رقیق اضافه کنید (به وسیله اسیدی کردن محلول ۱۰% NaCl با ۲/۰ حجمش HCl رقیق محلول آب کلر تهیه کنید) این محلول را به شدت تکان دهید اگر ید وجود داشته باشد فاز تتراکلرید کربن (فاز زیری) برنگ ارغوانی در می آید اگر افزایش آب کلر ادامه یابد رنگ ارغوانی ابتدا شدید تر شده و سپس رو به کاهش می گذارد و بالاخره ناپدید میگردد (اکسید شدن ید رنگی به یدات بی رنگ).
اگر در این آزمایش برم وجود داشته باشد لایه زیری به رنگ قهوه ای یا قرمز ظاهر میشود که با افزایش کلر این رنگ ناپدید نخواهد گشت. بروش فوق نمیتوان کلررا در جسم آلی تشخیص داد.
منابع:
۱)کتاب شیمی آلی تجربی نوین جلد دوم -نویسندگان:گیلبرت-ردوالد-وینگرو-ترجمه: هوشنگ پیر الهی
۲)کتاب شیمی آلی وعملی-مولفین:آقایان جلیلیان-وارسته مرادی-احمدی گلسفیدی
تست های شناسایی فنول ها
تست های شناسایی فنول ها
فنولها ترکیبات اسیدی هستند که قدرت اسیدی آنها از کربوکسیلیک اسیدها کمتر است این امر در مورد فنولهایی که دارای استخلافهای نیترو هستند صدق نمی کند. برخی از آزمایشهایی که در شناسایی فنولها مورد استفاده قرار می گیرد در زیر آمده است.
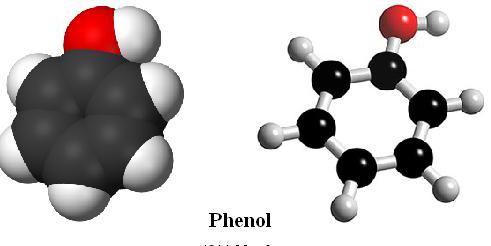
۱- محلول سدیم هیدروکسیدانحلال پذیری فنولها در محلول سیدم هیدروکسید، در مورد فنولهایی که امکان مزدوج شدگی در باز مزدوج (آنیون فنولات) آنها زیاد است، با رنگی شدن محلول همراه است. برای مشاهده رنگ، باید مقدار کمی از فنول را در محلول سدیم هیدروکسید ۱۰% حل نمود. انحلال بعضی فنولها با رنگی شدن همراه نیست. و تعدادی از آنها نیز در محلول سدیم هیدروکسید نامحلول هستند و بصورت رسوب می باشند.
۲- فریک کلرید فنولهای محلول در آب
چند قطره محلول آبی فریک کلرید ۵/۲% به یک میلی لیتر محلول آبی و رقیق فنول ( حدود ۳-۱% وزنی ) اضافه نمایید. در مورد بیشتر فنولها رنگ قرمز تند، آبی، ارغوانی یا سبز ظاهر می شد. بعضی رنگها بصورت گذرا هستند و برای مشاهده رنگ باید محلول خوب همزده شود و مخلوط گرد رنگی شدن معمولا فوری است. اما باید توجه داشت که رنگ محلول برای زمان زیادی پایدار نیست.
فنولهای نامحلول در آب بسیاری از فنولها با روشی که پیش از این ذکر شد و به آزمایش فریک کلرید پاسخ مثبت نمی دهند و باید آزمایش را بدین ترتیب انجام داد که ۲۰ میلی گرم از فنول جامد یا یک قطره فنول مایع را در یک میلی لیتر کلروفرم حل یا به حالت تعلیق درآورد و سپس یک قطره پیریدین و سه تا پنج قطره از محلول ۱ % فریک کلرید ( حجم/ وزن ) در کلروفرم به آن اضافه نمایید.
۳- برم / آب
محلول آبی ۱ % از مجهول تهیه نمایید سپس به آن قطره قطره محلول آب برم اشباع شده اضافه نمایید و هر بار تکان دهید تا رنگ زایل شود. تشکیل رسوب به دلیل تولید محصوص استخلاف شده است که همزمان با از بین رفتن رنگ برم است به عنوان نتیجه مثبت برای این آزمایش تلقی می شود.
تهیه مشتق ها
مشتقات فنولها اورتان ها هستند که از واکنش فنول با ایزوسیانات تولید می شود. مشتق های دیگر برای فنولها ۳ و ۵- دی نیترو بنزوآت و فنول برم دار شده است.
۱- ( α – نفتیل اورتان )۵/۰ گرم از فنول ( کاملاً خشک ) را در یک لوله آزمایش خشک بریزید و ۵/۰ میلی لیتر α – نفتیل ایزوسیانات به آن اضافه نمایید.
چند قطره پیریدین به عنوان کاتالیزور به مخلوط بیافزایید. اگر واکنش خود به خود صورت نگرفت، مخلوط را برای ۱۰-۵ دقیقه روی حمام بخار گرم نمایید. سپس لوله آزمایش را در بشر محتوی یخ قرار دهید و برای شروع تبلور با بهمزن شیشه یی خراش دهید. مایع روی رسوب تشکیل شده را جدا نمایید و در صورتیکه لازم است بلورها را روی بوخنر صاف نمایید. برای تخلیص محلول را در ۱۶-۵ میلی لیتر لیگروئین داغ (اتر نفت) یا هگزان حل کنید و برای جدا کردن مواد ناخواسته و دی فنیل اوره که ممکن است موجود باشد محلول را صاف نمایید ( قبلاً قیف را گرم کنید ). محلول صاف شده را سرد کنید تا اورتان متبلور شود. سپس بلورها را روی قیف بوخنر صاف نمایید.
۲- (۳ و ۵- دی نیترو بنزوآت)فنولهای مایع
۵/۰ گرم ۳ و ۵- دی نیترو بنزوئیل کلرید را در ۵/۰ میلی لیتر فنول حل نمایید و مخلوط را برای ۵ دقیقه حرارت دهید. بگذارید محلول سرد شود و سپس ۳ میلی لیتر محلول سدیم کربنات ۵ % و ۲ میلی لیتر آب به آن اضافه نمایید. مخلوط را بشدت بهم بزنید و چنانچه جامدی در مخلوط موجود است خرد نمایید. محصول را روی بوخنر صاف نمایید و با آب سرد بشویید. برای تخلیص آنرا بوسیله مخلوط حلال اتانول – آب متبلور نمایید.
فنولهای جامد
۵/۰ گرم فنول را در ۳ میلی لیتر پیریدین ( خشک ) حل نمایید و ۵/۰ گرم ۳ و ۵- دی نیترو بنزوئیل کلرید به آن اضافه کنید. مخلوط را برای ۱۵ دقیقه رفلاکس نمایید. بگذارید سرد شود و سپس آنرا به مخلوطی از ۵ میلی لیتر سدیم کربنات ۵ % و ۵ میلی لیتر آب اضافه کنید. سپس این مخلوط را در حمام یخ بگذارید و بشدت بهم بزنید تا تمام محصول واکنش بصورت بلورهایی تشکیل شود. رسوبها را با بوخنر صاف کنید و با آب سرد بشویید و برای تخلیص آنرا با مخلوط حلال اتانول – آب متبلور نمایید.
۳- بروموفنول
ابتدا چنانچه محلول برم آماده موجود نیست، باید آنرا از انحلال ۷۵/۰ گرم پتاسیم برومید در ۵ میلی لیتر آب و سپس ۵/۰ گرم برم تهیه نمایید. ۱/۰ گرم فنول را در یک میلی لیتر متانول یا دی اکسان حل کنید و سپس یک میلی لیتر آب اضافه نمایید. حال یک میلی لیتر مخلوط برم دار کننده را به مایع فنول بیافزایید و مخلوط را بشدت بچرخانید سپس افزایش محلول برم دار کننده را قطره قطره و در حالیکه مخلوط را می چرخانید ادامه دهید، محلول برم دار کننده را تا وقتی که رنگ محلول برم باقی بماند باید اضافه کرده ثابت ماندن رنگ برم در محلول، نشانه پایان واکنش برم دار کردن است. سپس باید ۵-۳ میلی لیتر آب اضافه کرد و مخلوط را بشدت تکان داد رسوبها را روی قیف بوخنر صاف نمایید و با اب بخوبی بشویید. برای تخلیص مشتق تهیه شده آنرا بوسیله مخلوط حلال متانول – آب متبلور نمایید.
پیوند آروماتیک
پیوند آروماتیک
پیوند آروماتیک به یک پیوند آلی گفته میشود که در آن یک حلقه جفت از پیوندهای غیراشباع، جفتهای تکی یا اربیتالهای خالی یک استواری قویتر از استواری جفتسازی تنها را از خود نشان میدهند.
واژه آروماتیک به معنی خوشبو است.
آروماتیکها، دسته وسیعی از ترکیبات را تشکیل میدهند که شامل بنزن و ترکیباتی باشند که از نظر رفتار شیمیایی مشابه بنزن میباشند. برخی از این مواد، حتی به ظاهر شباهتی به بنزن ندارند. برخلاف آلکنها و آلکینها، بنزن و سایر ترکیبات آروماتیک، تمایلی برای انجام واکنشهای افزایش از خود نشان نمیدهند، ولی در واکنشهای جانشینی شرکت میکنند که یکی از صفات شاخص این دسته از مواد میباشد.
اگر گروههای عاملی روی حلقه قرار بگیرند، بر واکنش پذیری حلقه اثر خواهند گذاشت. واکنش پذیری عوامل متصل به حلقه نیز به وسیله بخش آروماتیک تحتتأثیر قرار میگیرد.
مولکولهایی آروماتیک هستند و خصلت آروماتیکی از خود نشان میدهند که تعداد الکترونهای سیستم π آنها، ۲ و ۴ و ۶و ۱۰و… باشد. این ضرورت، قاعده هوکل یا ۴n+۲ نامیده میشود. سپس ترکیباتی که برای آنها n=0, ۱ , ۲ ,… میباشد، آروماتیک خواهند بود.
اگر گروههای عاملی روی حلقه قرار بگیرند، بر واکنش پذیری حلقه اثر خواهند گذاشت. واکنش پذیری عوامل متصل به حلقه نیز به وسیله بخش آروماتیک تحت تأثیر قرار میگیرد.
خصلت آروماتیکی و قاعده ۴n+۲ هوکل افزون بر بنزن و ترکیبات هم خانواده آن مثل نفتالین و آنتراسین و…، مواد دیگری نیز وجود دارند که بهظاهر هیچ شباهتی به بنزن ندارند، ولی رفتاری مشابه بنزن دارند و بهعبارت ساده تر، آروماتیک هستند. از ویژگیهای این مواد میتوان به نکات زیر اشاره نمود:
۱. گرمای هیدروژن دار شدن و گرمای سوختن آنها پایین است.
۲. برای انجام واکنشهای افزایشی، تمایل زیادی نشان نمیدهند.
۳. در واکنشهای جانشینی الکترونخواهی شرکت میکنند. بررسیهای تجربی مثل مطالعه خواص فیزیکی و انرژی هیدروژندار شدن سیستمها با تعداد الکترونهای π مختلف به این نتایج منجر شدهاست که:
۱. مولکولهایی آروماتیک هستند و خصلت آروماتیکی از خود نشان میدهند که تعداد الکترونهای سیستم π آنها، ۲ و ۶و ۱۰و… باشد. این ضرورت، قاعده هوکل یا ۴n+۲ نامیده میشود. سپس ترکیباتی که برای آنها n=0, ۱ , ۲ ,… میباشد، آروماتیک خواهند بود.
۲. مولکول باید ساختمان مسطح داشته باشد. تمام ترکیباتی که این دو شرط اساسی در آنها رعایت شده باشد، زوایای پیوندی در آنها طبیعی، همپوشانی اوربیتالهای π مناسب و غیر مستقر شدن الکترونها بخوبی میسر باشد، پایداری مولکول بیشتر خواهد بود. یک مثال واکنش
۳- کلرو سیکلوپروپن با SbCl۵، ماده پایداری به فرمول C3H۳SbCl۶ ایجاد میکند که در حلالهای دیاکسید گوگرد مایع بخوبی حل نشده، ولی در حلالهای غیرقطبی نامحلول است. مطالعه طیفNMR این ماده، سه پروتون همارزش را به نمایش میگذارد. این نتایج، با تشکیل کاتیون سیکلوپروپن که کوچکترین مولکول آروماتیک میباشد، مطابقت دارد. ترکیبهای آروماتیک، هتروآروماتیک و انرژی رزونانس نتایج تجربی حاصل از واکنشهای هیدروژن دار شدن هیدروکربنهای جوش خورده دو حلقهای و سه حلقهای و… نشان میدهد که هر چه تعداد الکترونهای بیشتری در رزونانس شرکت کرده باشند، انرزژی آزاد شده بیشتر و پایداری نسبی نیز بیشتر خواهد بود.
نامگذاری مشتقات بنزن و ترکیبات آروماتیک جوش خورده برخی از مشتقات بنزن، نام مخصوص به خود دارند، مثلاً هیدروکسی بنزن را فنول (C6H۵OH)، متوکسی بنزن را آنیزول (C6H۵OCH3)، متیل بنزن را تولوئن (C6H۵CH3)، ایزوپروپیل بنزن را کیومن و آمینوبنزن را آنیلین میگویند.
برای نامگذاری خیلی از مشتقات بنزن، نام گروه یا استخلاف به صورت پیشوند بر کلمه بنزن افزوده میشود. مثلاً فلوئورو بنزن، ترسیوبوتیل بنزن، نیتروبنزن، سیکلوپروپیل بنزن نمونههایی از این نوع هستند. جهت نامگذاری مشتقات دو استخلافی بنزن. لازم است که محل استخلافها از پیشوند اورتو، متا یا پارا استفاده شود؛ به عنوان مثال، اورتو دیمتیل بنزن، متا دیمتیل بنزن، پارا دیمتیل بنزن.
در مواردیگه دو استخلاف متفاوت روی حلقه بنزن قرار گرفته باشد و هیچکدام از گروهها نام ویژهای به مولکول نداده باشند، پس از ذکر موقعیت گروهها با پیشوند اورتو و…، نام گروهها را ذکر نموده، در پایان، کلمه بنزن بر آنها افزوده میشود. اگر وجود یک گروه، نام ویژهای به مولکول بدهد، در آن صورت مولکول به عنوان مشتق آن ترکیب ویژه محسوب میشود.
پارافین
پارافین – Paraffin
اولین نوع عمده نفت خام، پارافین ها هستند که آلکینز (alkanes )نیز نامیده می شوند. فرمول کلی پارافین ها CnH2n+2 می باشد. ساده ترین و سبک ترین مولکول سری پارافین ها، متان با فرمول CH4 است. پارافین های با کمتر از پنج اتم کربن، در فشار و حرارت عادی به شکل گازی هستند. علاوه بر متان، دیگر پارافین های گازی عبارتند از اتان، پروپان و بوتان. برای سادگی اینها گاهی اوقات C1 تا C4 نیز نامیده می شوند. از C5 تاC15 پارافین ها در حرارت و فشار عادی مایع هستند. هیدروکربن های با بیشتر از ۱۵ اتم کربن (C15)، به شدت گرانرو یا ویسکوز هستند و حالت واکس های جامد را به خود می گیرند. انواع پارافین ها تا C40 و بالاتر از آن مشاهده می شوند.
پارافین واکس به عنوان یک محصول جانبی در پالایشگاههای تولید روغن به دست می آید و بسته به نوع برش نفتی روغن پالایش شده دارای گریدهای مختلفی می باشد. از جمله خواص بارز پارافین واکس مقاومت بالای آن در مقابل آب و بخار بوده که همین خصوصیت باعث گردیده تا به عنوان پوششهای محافظ روی کاغذ نیز مورد استفاده قرار گیرد. پارافین واکس در مقابل بسیاری از اسیدها و قلیاها مقاوم بوده و پوشش مناسبی به عنوان محافظ خوردگی بشکه ها و مخازن صنعتی می باشد. علاوه بر این بدلیل دارا بودن خواص قابل توجهی به عنوان عایق الکتریکی دارای کاربردهای فراوانی بوده و در صنایع مختلف از جمله نساجی نیز مورد مصرف می باشد.

موارد کاربرد:
· شمع سازی
· تولید پارچه و کاغذهای صنعتی ضد آب
· واکس های صنعتی
· مرکب های جامد کاغذ کپی
· کبریت سازی
· پایه محصولات روانکاری و وازلین
بزرگترین تقاضا برای پارافینهای نرمال ، تولید شویندههای فروپاشی پذیر بروش زیستی ( biodegradable )است. این پارافینها بعنوان خوراک صنایع پتروشیمی استفاده میشوند.
سیکلوپارافین یا نفتن
هیدروکربنهای سیکلوپارافینی که تمام پیوندهای آزاد اتمهای کربن آنها با هیدروژن ، سیر شدهاند، نفتن نامیده میشوند. در نفت خام ، انواع بسیاری از نفتنها وجود دارد. ولی بجز در مورد ترکیبهای دارای جرم مولکولی اندک ، نظیر سیکلوپنتان و سیکلوهگزان ، معمولا بصورت ترکیبهای جداگانه تفکیک نمیشوند.طبقه بندی آنها با توجه به گستره نقاط جوش صورت میگیرد و خواص آنها بکمک عوامل همبستگی نظیر عامل Kw یا CI تعیین میشود.
پارافین مایع:
این محصول بر اساس استانداردهای BPوUSP تولید شده و به علت خلوص و پایداری بالا در صنایع مختلف مورد مصرف دارد.
درجه A:دارویی
درجه B:بهداشتی
درجه C: صنعتی
موارد مصرف:
روغن مو،کرم پاک کننده ،کرم سرد، عامل ضد گرد و غبار ،روغن کاری صنایع نساجی ،روکش تخم مرغ و میوه های تازه.این محصول با مشخصه بدون بو، بدون رنگ و بدون مزه قابل حل در حلالهای طبیعی و نامحلول در آب و الکل است و به همین علت بصورت گسترده در صنایع مصرف دارد.
پارافین صنعتی
فرایند تولیدی پارافین صنعتی ممکن است به یکی از روشهای ذیل باشد:
الف-فرایند اسیدی :در این روش اسلاک واکس بعد از ذوب مجدد و داخل کردن اسید بدون حلال بطور سرد توسطسانتریفوژ عمل جداسازی پارافین ناخالص صورت می گیرد.بعداز این عمل محصول را خشک نموده و با اسید سولفوریکتصفیه می نمایند. برای زدودن نا خالصی ها توسط خاک نیز تصفیه نهایی انجام شده و پس از فیلتراسون قاب گیری وبالاخره بسته بندی می شوند.
ب- فرایند تعریق : در این روش اسلاک واکس بعد از قالب گیری اولیه و روغن گیری به روش تعریق و تصفیه با اسیدسولفوریک عملیات بعدی به روش همان فرایند اسیدی (از مرحله تصفیه به بعدانجام )ادامه می یابد.
پارافین کلره
به گروهی از مواد شیمیایی با ارزش اطلاق می شود که در صنایع پلیمر به ویژه در PVC به عنوان نرم کننده (Plasticize، به تاخیر اندازنده اشتعال (Flame retardant)برای پلاستیک ها و لاستیک ها، بعنوان کاهش دهنده نقطه ریزش ( Pour Point depressant) در رنگها و نیز ماده افزودنی برای روغن موتور فشار بالا (Extreme pressure additive)، کاربرد وسیعی دارد و سالانه صدها هزار تن از این ماده در دنیا تولید و به مصرف می رسد. در داخل کشور پارافین کلره ۵۲ درصدی به عنوان یکی از گریدهای پر مصرف به تنهایی و یا در کنار DOP در صنایع کابل سازی، چرم مصنوعی، کف پوش و … به عنوان نرم کننده کاربرد فراوان دارد. )
تولید پارافینهای نرمال در پالایشگاه
پارافینهای نرمال به روش جذب فاز بخار برشهای نفتی بر روی غربالهای مولکولی با میانگین تخلخل ۵ آنگستروم بدست میآیند. جذب در فاز بخار در فشارهای پنج تا ده psig ( سی و پنج تا شصت و نه KPa )و در دمای ۳۰۰ تا ۳۵۰ درجه سانتیگراد یا ۵۷۵ تا ۶۵۰ درجه فارینهایت انجام میشود. از آمونیاک برای جذب پارافینهای نرمال استفاده میشود.
عملیات نیمه مداوم با استفاده از دو بستر غربال مولکولی پنج آنگستروم این امکان را میدهد که یک بستر برای جذب بکار گرفته شود و بستر دیگر در حال واجذب باشد. غربال مولکول بتدریج ظرفیت خود را بدلیل آلودگی با فراورده های بسیاری از دست میدهد که آنگاه با احتراق کنترل شده هیدروکربنهای سنگین احیا میشود. معمولا احیا پس از ۱۲ ماه فعالیت غربال مولکولی انجام میپذیرد.
منبع: شیمی گست
آزمایش کوپلیمریزاسیون رادیکالی
آزمایش کوپلیمریزاسیون رادیکالی
هدف آزمایش
تهیه کوپلیمری دارای خصوصیات بهتری از پلی متیل- متاکریلات و پلی آکریلونیتریل
تئوری آزمایش
کوپلیمرها را در صنعت برای بهتر نمودن خواص مواد بکار میبرند. بعنوان مثال ، هموپلیمری (پلیمری با فقط یک نوع منومر) برای کاربرد بخصوص ، دارای خواص مناسبی میباشد، ولی یک یا چند خصلت آن ، زیاد مناسب نیست. در این هنگام ، کوپلیمری درست میکنند که خصلتهای نامساعد را بهبود بخشد. بعنوان مثال ، پلی پروپیلن ایزوتاکتیک ، پلیمر با قدرت مکانیکی خوبی است، ولی قدرت رنگپذیری ندارد. برای از بین بردن این نقیصه ، پروپیلن را هنگام کوپلیمریزاسیون با یک منومر دیگر ، کوپلیمره میکنند.
اکریلونیتریل بعنوان الیاف و با نام “اورلون” کاربرد دارد. آفینیته رنگرزی در این مولکول پایین میباشد، یعنی تمایل به گرفتن رنگ پایین است. برای بالا بردن آفینیته رنگرزی ، به مقدار کم با اسید اکریلیک (حدود %۱۰) کوپلیمریزه میکنند. گروه اسیدکربوکسیلیک تمایل به گرفتن رنگ را در اورلون زیاد میکند، بدون اینکه به خواص دیگر پلی اکریلونیتریل صدمه بزند.
وسایل لازم
- لوله آزمایش ۵۰ میلی لیتری که بوسیله شعله از قسمت دهانه کشیده شده است.
- بالن ۱۰۰ میلی لیتری
- مبرد
- حمام آبی
- متیل متاکریلات
- آکریلونیتریل
- بنزوئیل پراکسید و یا AIBN
- استون
- الکل متیلیک و یا الکل اتیلیک
روش آزمایش
داخل لوله آزمایشی که از قسمت دهانه (با شعله) کشیده شده است، ۱۰ گرم ، متیل متاکریلات ، ۵ گرم ، آکریلونیتریل و ۰,۰۵ گرم ، آغازگر ریخته و بادقت ، دهانه لوله آزمایش را با شعله میبندند. سپس لوله را با زرورق آلومینیومی پیچیده و بمدت ۴ ساعت در حمام آبی به دمای ۸۰ درجه سانتیگراد قرار میدهند. بعد از زمان مقرر ، لوله آزمایش را خارج نموده و پس از سرد شدن ، دهانه آن را بدقت شکسته و کوپلیمر حاصل را با یخ سرد کرده و بروش مکانیکی به تکه های کوچکتر تبدیل میکنند.
این تکه های کوچک را بهمراه استون در بالنی که به سر آن مبردی متصل شده، تحت تاثیر حرارت ، حل میکنند. بعد از سرد شدن محلول ، بوسیله الکل متیلیک و یا الکل اتیلیک (اتانول)، کوپلیمر را رسوب میدهند و در اتو خلاء در دمای ۴۰ درجه سانتیگراد خشک کرده و توزین میکنند.
حمام آبی ظرفی است که در آن ، آب در حال جوشیدن است و ظرف مورد حرارت در روی آن ، تحت حرارت غیر مستقیم قرار دارد. اتو خلاء ، ظرفی است که مواد شیمیایی را در آن ، در شرایط بدون هوا و اکسیژن ، خشک میکنند.
نتیجه
تهیه کوپلیمر فوق (با توجه به روش کار) به دقت بسیار زیادی نیاز دارد. عدم رسیدن هوا برای رسیدن به ماده مورد نظر بسیار مهم است. کوپلیمر حاصل در ضمن در استون قابل حل است. کوپلیمر فوق ، برای بهتر کردن خصوصیات مکانیکی پلیمر پلی اکریلونیتریل و رنگپذیری بهتر مناسب است. بدون اینکه خواص پلی اکریلونیتریل دچار اشکال گردد.
آزمایش کوپلیمریزاسیون رادیکالی
آزمایش کوپلیمریزاسیون رادیکالی
هدف آزمایش
تهیه کوپلیمری دارای خصوصیات بهتری از پلی متیل- متاکریلات و پلی آکریلونیتریل
تئوری آزمایش
کوپلیمرها را در صنعت برای بهتر نمودن خواص مواد بکار میبرند. بعنوان مثال ، هموپلیمری (پلیمری با فقط یک نوع منومر) برای کاربرد بخصوص ، دارای خواص مناسبی میباشد، ولی یک یا چند خصلت آن ، زیاد مناسب نیست. در این هنگام ، کوپلیمری درست میکنند که خصلتهای نامساعد را بهبود بخشد. بعنوان مثال ، پلی پروپیلن ایزوتاکتیک ، پلیمر با قدرت مکانیکی خوبی است، ولی قدرت رنگپذیری ندارد. برای از بین بردن این نقیصه ، پروپیلن را هنگام کوپلیمریزاسیون با یک منومر دیگر ، کوپلیمره میکنند.
اکریلونیتریل بعنوان الیاف و با نام “اورلون” کاربرد دارد. آفینیته رنگرزی در این مولکول پایین میباشد، یعنی تمایل به گرفتن رنگ پایین است. برای بالا بردن آفینیته رنگرزی ، به مقدار کم با اسید اکریلیک (حدود %۱۰) کوپلیمریزه میکنند. گروه اسیدکربوکسیلیک تمایل به گرفتن رنگ را در اورلون زیاد میکند، بدون اینکه به خواص دیگر پلی اکریلونیتریل صدمه بزند.
وسایل لازم
- لوله آزمایش ۵۰ میلی لیتری که بوسیله شعله از قسمت دهانه کشیده شده است.
- بالن ۱۰۰ میلی لیتری
- مبرد
- حمام آبی
- متیل متاکریلات
- آکریلونیتریل
- بنزوئیل پراکسید و یا AIBN
- استون
- الکل متیلیک و یا الکل اتیلیک
روش آزمایش
داخل لوله آزمایشی که از قسمت دهانه (با شعله) کشیده شده است، ۱۰ گرم ، متیل متاکریلات ، ۵ گرم ، آکریلونیتریل و ۰,۰۵ گرم ، آغازگر ریخته و بادقت ، دهانه لوله آزمایش را با شعله میبندند. سپس لوله را با زرورق آلومینیومی پیچیده و بمدت ۴ ساعت در حمام آبی به دمای ۸۰ درجه سانتیگراد قرار میدهند. بعد از زمان مقرر ، لوله آزمایش را خارج نموده و پس از سرد شدن ، دهانه آن را بدقت شکسته و کوپلیمر حاصل را با یخ سرد کرده و بروش مکانیکی به تکه های کوچکتر تبدیل میکنند.
این تکه های کوچک را بهمراه استون در بالنی که به سر آن مبردی متصل شده، تحت تاثیر حرارت ، حل میکنند. بعد از سرد شدن محلول ، بوسیله الکل متیلیک و یا الکل اتیلیک (اتانول)، کوپلیمر را رسوب میدهند و در اتو خلاء در دمای ۴۰ درجه سانتیگراد خشک کرده و توزین میکنند.
حمام آبی ظرفی است که در آن ، آب در حال جوشیدن است و ظرف مورد حرارت در روی آن ، تحت حرارت غیر مستقیم قرار دارد. اتو خلاء ، ظرفی است که مواد شیمیایی را در آن ، در شرایط بدون هوا و اکسیژن ، خشک میکنند.
نتیجه
تهیه کوپلیمر فوق (با توجه به روش کار) به دقت بسیار زیادی نیاز دارد. عدم رسیدن هوا برای رسیدن به ماده مورد نظر بسیار مهم است. کوپلیمر حاصل در ضمن در استون قابل حل است. کوپلیمر فوق ، برای بهتر کردن خصوصیات مکانیکی پلیمر پلی اکریلونیتریل و رنگپذیری بهتر مناسب است. بدون اینکه خواص پلی اکریلونیتریل دچار اشکال گردد.
تهیه پلی متیل متاکریلات به روش نوری
تهیه پلی متیل متاکریلات به روش نوری
بطور کلی ، پلیمریزاسیون زنجیری به واکنش ترکیب مولکولهای منومر با یکدیگر و تشکیل مولکولهای بزرگ پلیمری گفته میشود. در این روش ، تغییری در ترکیب عنصری بوجود نمیآید و در روند پلیمریزاسیون به هیچ وجه ، محصول جانبی بدست نمیآید. واکنش پلیمریزاسیون زنجیری برای ترکیباتی که دارای یک یا چند بند سیر نشده میباشند، مورد استفاده قرار میگیرد.
پلیمریزاسیون ، تنها مختص ترکیباتی که در آنها ، بند دوگانه بین دو اتم کربن واقع است، نمیباشد، بلکه در مورد بندهای دوگانه مابین کربن و عنصر دیگر نیز بوقوع میپیوندد. این مورد ، حالتی استثنایی میباشد و در این مقوله ، تنها بذکر پلیمریزاسیون ترکیباتی که بند دوگانه مابین دو اتم کربن قرار دارد توجه داریم. در این روش ، بعلت بالا بودن سرعت واکنش نسبت به روشهای دیگر ، میتوان به اجرام بسیار بالایی دست یافت.
وسایل مورد نیاز
- ۴ لوله آزمایش که بوسیله شعله از قسمت وسط کشیده شدهاند.
- ۴ عدد بشر ۱۰۰ میلی لیتری
- لامپ جیوه
- پایه فلزی
- متیل متاکریلات
- بنزن
- اتر نفت
- هپتان و یا هگزان
روش آزمایش
داخل چهار لوله آزمایش ، ۵ گرم ( ۵,۳ میلی لیتر ) ، متیل متاکریلات میریزیم. بکمک شعله ، دهانه لولههای آزمایش را بادقت میکشیم و میبندیم و به پایه فلزی متصل میکنیم. بوسیله لامپ جیوهای ، لوله آزمایش شماره ۱ ( لولههای آزمایش را شمارهگذاری کردهایم ) را بمدت دو ساعت ، لوله آزمایش شماره ۲ را بمدت چهار ساعت ، لوله آزمایش شماره ۳ را بمدت شش ساعت و لوله آزمایش شماره ۴ را بمدت هشت ساعت ، تحت تشعشع قرار میدهیم.
بعد از پایان موعد مقرر ، دهانه لولههای آزمایش را بدقت باز میکنیم. بر روی هر کدام از لولههای آزمایش ، ۲۰ میلی لیتر بنزن ریخته و پلی متیل متاکریلات حاصل شده را در آن حل میکنیم. بعد از انحلال ، پلیمر را بداخل بشرهای ۱۰۰ میلی لیتری منتقل میکنیم و بکمک ۵۰ الی ۶۰ میلی لیتر اتر نفت ، هپتان و یا هگزان ، پلیمر را رسوب میدهیم. رسوب پلی متیل متاکریلات را بدقت جدا می کنیم.
نتیجه آزمایش
پلیمر پلی متیل متاکریلات از طریق پلیمریزاسیون زنجیری حاصل شد که در اینجا ، بطریق پلیمریزاسیون نوری بود. پلیمر حاصل در سرویسهای حمام و همینطور در لنزها مورد استفاده قرار میگیرد.
تهیه پلی متیل متاکریلات به روش نوری
تهیه پلی متیل متاکریلات به روش نوری
بطور کلی ، پلیمریزاسیون زنجیری به واکنش ترکیب مولکولهای منومر با یکدیگر و تشکیل مولکولهای بزرگ پلیمری گفته میشود. در این روش ، تغییری در ترکیب عنصری بوجود نمیآید و در روند پلیمریزاسیون به هیچ وجه ، محصول جانبی بدست نمیآید. واکنش پلیمریزاسیون زنجیری برای ترکیباتی که دارای یک یا چند بند سیر نشده میباشند، مورد استفاده قرار میگیرد.
پلیمریزاسیون ، تنها مختص ترکیباتی که در آنها ، بند دوگانه بین دو اتم کربن واقع است، نمیباشد، بلکه در مورد بندهای دوگانه مابین کربن و عنصر دیگر نیز بوقوع میپیوندد. این مورد ، حالتی استثنایی میباشد و در این مقوله ، تنها بذکر پلیمریزاسیون ترکیباتی که بند دوگانه مابین دو اتم کربن قرار دارد توجه داریم. در این روش ، بعلت بالا بودن سرعت واکنش نسبت به روشهای دیگر ، میتوان به اجرام بسیار بالایی دست یافت.
وسایل مورد نیاز
- ۴ لوله آزمایش که بوسیله شعله از قسمت وسط کشیده شدهاند.
- ۴ عدد بشر ۱۰۰ میلی لیتری
- لامپ جیوه
- پایه فلزی
- متیل متاکریلات
- بنزن
- اتر نفت
- هپتان و یا هگزان
روش آزمایش
داخل چهار لوله آزمایش ، ۵ گرم ( ۵,۳ میلی لیتر ) ، متیل متاکریلات میریزیم. بکمک شعله ، دهانه لولههای آزمایش را بادقت میکشیم و میبندیم و به پایه فلزی متصل میکنیم. بوسیله لامپ جیوهای ، لوله آزمایش شماره ۱ ( لولههای آزمایش را شمارهگذاری کردهایم ) را بمدت دو ساعت ، لوله آزمایش شماره ۲ را بمدت چهار ساعت ، لوله آزمایش شماره ۳ را بمدت شش ساعت و لوله آزمایش شماره ۴ را بمدت هشت ساعت ، تحت تشعشع قرار میدهیم.
بعد از پایان موعد مقرر ، دهانه لولههای آزمایش را بدقت باز میکنیم. بر روی هر کدام از لولههای آزمایش ، ۲۰ میلی لیتر بنزن ریخته و پلی متیل متاکریلات حاصل شده را در آن حل میکنیم. بعد از انحلال ، پلیمر را بداخل بشرهای ۱۰۰ میلی لیتری منتقل میکنیم و بکمک ۵۰ الی ۶۰ میلی لیتر اتر نفت ، هپتان و یا هگزان ، پلیمر را رسوب میدهیم. رسوب پلی متیل متاکریلات را بدقت جدا می کنیم.
نتیجه آزمایش
پلیمر پلی متیل متاکریلات از طریق پلیمریزاسیون زنجیری حاصل شد که در اینجا ، بطریق پلیمریزاسیون نوری بود. پلیمر حاصل در سرویسهای حمام و همینطور در لنزها مورد استفاده قرار میگیرد.
شیمی آلی، ویژگی ها و ترکیبات
شیمی آلی، ویژگی ها و ترکیبات
شیمی آلی زیر مجموعه ای از دانش شیمی است که درباره ترکیبات کربن یا مواد آلی سخن میگوید، عنصر اصلی که با کربن ترکیبات آلی را تشکیل می دهند، هیدروژن می باشد. در گذشته به موادی که ریشه گیاهی یا حیوانی داشتند، مواد آلی می گفتند اما امروزه مواد آلی را می توان از طریق روش های صنعتی و آزمایشگاهی و به کمک مواد معدنی نیز سنتز کرد. موادی که از منابع آلی بدست می آیند، در یک ویژگی مشترک هستند و آن اشتراک در دارا بودن عنصر کربن است. دو منبع بزرگ مواد آلی که از آنها مواد آلی با ترکیبات ساده، تأمین می شوند، نفت و زغال سنگ هستند، این دو ماده فسیلی در مفهوم قدیمی آلی بوده و حاصل تجزیه جانوران و گیاهان هستند. این ترکیبات ساده به عنوان مصالح ساختمانی، در ساختن ترکیبات بزرگتر و پیچیده تر مصرف می گردند. شیمی آلی، شیمی ترکیبات کربن با سایر عناصر به ویژه هیدروژن، اکسیژن، نیتروژن، هالوژن ها و غیر فلزات دیگر نظیر گوگرد و منیزیوم است. الکل ها، اترها، هیدروکربن ها، آلدئیدها، کتون ها، کربوکسیلیک اسیدها، ترکیبات آلیفاتیک حلقوی، کربانیون ها، آمین ها، فنل ها، درشت مولکول ها و بسپارها (پلیمر) و نظیر آنها جزء مواد آلی بوده و مباحث شیمی آلی را به خود اختصاص داده اند. امروزه از مواد آلی و دانش شیمی آلی در رنگ سازی، کاغذ و جوهرسازی، مواد غذایی، پوشاک، پتروشیمی، مواد پلاستیکی و لاستیکی، داروسازی، پزشکی و ده ها صنعت دیگر بهره می برند. افزون بر بیست میلیون ترکیب شناخته شده کربن وجود دارد و هر ساله نیم میلیون ملکول جدید به خانواده مواد آلی اضافه می شوند. شیمی آلی شالوده زیست شناسی و پزشکی است. ساختمان موجودات زنده به غیر از آب، عمدتا” از مواد آلی ساخته شده اند، مولکول های مورد بحث در زیست شناسی مولکولی همان مولکول های آلی هستند. امروزه ما در عصر کربن زندگی می کنیم، هر روزه روزنامه ها و مجلات، ذهن ما را متوجه ترکیبات کربن نظیر کلسترول، چربی های اشباع نشده، هورمون ها، استروئیدها، حشره کش ها و فرومون ها می نماید. در دهه های گذشته به خاطر نفت جنگ های متعددی راه افتاده است، همچنین دو فاجعه نازک شدن لایه اوزون که عمدتا” به خاطر وجود کلرو فلوئورو کربن ها می باشد و پدیده گازهای گلخانه ای که ناشی از حضور متان، کلرو فلوئورو کربن ها و دی اکسید کربن است، زندگی انسان ها را به خطر انداخته است.

آرایش و درشتی مولکول های مواد آلی
تا حدود سال ۱۸۵۰ میلادی بسیاری از دانشمندان بر این باور بودند که منشأ مواد آلی، جانداران و گیاهان هستند، آنها تصور می کردند که مواد آلی را هرگز نمی توان از مواد معدنی و غیر آلی تولید نمود. دانشمندان همواره دنبال پاسخ به این پرسش بودند که چه ویژگی در ترکیبات کربن وجود دارد که آنها را از ترکیبات مربوط به صد و چند عنصر دیگر جدول تناوبی متمایز کرده است. تعداد بسیاری از ترکیبات کربن وجود دارند که مولکول های آنها می توانند بسیار بزرگ و پیچیده باشند. تعداد ترکیباتی که دارای عنصر کربن هستند چندین برابر بیشتر از تعداد ترکیبات بدون کربن است. مولکول های آلی شامل هزاران اتم شناخته شده اند و ترتیب قرار گرفتن اتم ها حتی در مولکول های نسبتا” کوچک نیز بسیار پیچیده است. یکی از مسائل اصلی در شیمی آلی، آگاهی از طرز قرار گرفتن اتم ها در مولکول ها و یا تعیین ساختمان ترکیبات است.
ویژگی منحصر به فرد اتم کربن
اتم های کربن می توانند به میزانی که برای اتم هیچ عنصر دیگری مقدور نیست، به یکدیگر متصل شوند. همچنین اتم های کربن می توانند زنجیرهایی شامل هزاران اتم و یا حلقه هایی با اندازه های متفاوت ایجاد نمایند، زنجیرها و حلقه ها می توانند دارای شاخه و پیوندهای عرضی باشند، به اتم های کربن این زنجیرها و حلقه ها، اتم های دیگری نیز می تواند وصل شود، این اتم ها معمولا” هیدروژن، فلوئور، کلر، برم، ید، اکسیژن، نیتروژن، گوگرد، فسفر و سایر اتم های مختلف می باشند. هر آرایش مختلف از اتم ها مربوط به ترکیب متفاوتی است و هر ترکیب یک سری خواص شیمیایی و فیزیکی خاص خود را دارد، از این رو غیر منتظره نیست که امروزه ده ها میلیون ترکیب شناخته شده کربن وجود داشته باشد.
پیوند شیمیایی
بررسی ساختمان مولکول ها را باید با بحث درباره پیوندهای شیمیایی یعنی نیروهایی که اتم ها را در یک مولکول نگاه می دارند، شروع نمود. دو نوع پیوند یونی و کووالانسی، پیوندهایی هستند که به وسیله آن اتم ها با یکدیگر اتصال برقرار می کنند. از میان این دو پیوند، پیوند کووالانسی، پیوند متدوال در ترکیبات کربن است و مهمترین پیوند در مطالعه شیمی آلی است.
مواد آلی در شیمی آلی
مواد آلی دارای گستره ای بزرگ می باشند و بسیار متفاوت و متنوع هستند. از این دسته مواد می توان، پارافین ها، روغن ها، هیدرو کربن ها، الفین ها، استیلن ها، ترپن ها، الکل ها، اسیدهای کربوکسیلیک، استرها، اترها، اپوکسیدها، آلدئیدها، کتون ها، آمین ها، آمیدها، ترکیبات آروماتیک، اسیدهای آلی، ایزوسیونات ها، محصولات استخلافی بنزن، الیاف نساجی، رنگ های رنگرزی و صنعتی و … را نام برد.
ترکیبات هیدرو کربنی
برخی از ترکیبات آلی فقط شامل دو عنصر، هیدروژن و کربن هستند و از این رو به عنوان هیدرو کربن شناخته می شوند. هیدرو کربن ها بر اساس ساختمان شان، به دو دسته اصلی، آلیفاتیک و آروماتیک تقسیم می شوند. هیدرو کربن های آلیفاتیک خود به گروه های آلکان ها، آلکن ها، آلکین ها و ترکیبات حلقه ای مشابه سیکلو آلکان ها و غیره تقسیم می گردند.
متان
ساده ترین ماده شیمی آلی متان است، مولکول متان دارای یک اتم مرکزی کربن و چهار اتم محیطی هیدروژن است که با زاویه ۱۰۹/۵ درجه دور اتم کربن قرار گرفته اند. متان محصول نهایی متلاشی شدن ناهوازی (بدون هوا) گیاهان یعنی از هم پاشیدگی بعضی از مولکول های پیچیده می باشد. متان تشکیل دهنده قسمت اعظم (حدود ۹۷ درصد) گاز طبیعی است. متان گاز آتشگیر خطرناک معادن زغال سنگ است و به صورت حباب های گاز از سطح مرداب ها خارج می گردد. گاز متان از ترکیب مونو اکسید کربن و هیدروژن حاصل می گردد.
کلرو فلوئورو کربن ها
مشتقات هالوژنه متان را کلرو فلوئورو کربن ها می گویند. اگر به جای هیدروژن های متان اتم های هالوژن جایگزین گردد، این محصولات حاصل می شوند. گازهای مورد استفاده در یخچال ها و کولرهای گازی و انواع اسپری، از این دسته مواد هستند. از جمله این مواد می توان به دی کلرو دی فلوئورو متان و کلرو تری فلوئورو متان اشاره کرد.
CF2Cl2 یا CFC12 دی کلرو دی فلوئورو متان
CF3Cl یا CFC11 کلرو تری فلوئورو متان
آلکان ها
آلکان ها که نقطه آغازگر آن ها متان است به ترکیبات غیر حلقوی و خطی کربن و هیدروژن اطلاق می شود، پیوند یگانه کووالانسی در این ترکیبات اتم های کربن و هیدروژن را به هم وصل کرده است. این هیدرو کربن ها بر اساس ساختمانشان به خانواده متان تعلق دارند و خواص آنها از خواص متان پیروی می کند. در آلکان ها تعداد اتم های هیدروژن نسبت به اتم های کربن، دو برابر به علاوه دو می باشد. یعنی مثلا” در مولکول بوتان، چهار اتم کربن و ده اتم هیدروژن وجود دارد. در آلکان ها، انتظار می رود هرچه تعداد اتم ها افزایش یابد، تعداد آرایش های ممکن اتم ها نیز زیادتر می شود. به تدریج که در سری آلکان ها پیش می رویم، تعداد ایزومرها در همرده های متوالی به میزان شگفت آوری افزایش می یابند. برای مثال هپتان دارای نه ایزومر می باشد، یعنی در شیمی آلی نه ماده مختلف با خواص متفاوت هستند که همگی فرمولشان C7H16 است. برای نامیدن ترکیبات مختلف و پیچیده آلی از روش استاندارد آیوپاک استفاده می کنند.
منابع
کتب شیمی آلی
شیمی آلی، جلد اول نوشتهٔ موریسون و بوید، ترجمهٔ علی پور جوادی
شیمی آلی، جلد دوم نوشتهٔ موریسون و بوید، ترجمهٔ علی پور جوادی
شیمی آلی، نوشتهٔ گراهام ت. سولومونز، ترجمهٔ سلاجقه، هروی و عبدی اسکویی
شیمی آلی، ویژگی ها و ترکیبات
شیمی آلی، ویژگی ها و ترکیبات
شیمی آلی زیر مجموعه ای از دانش شیمی است که درباره ترکیبات کربن یا مواد آلی سخن میگوید، عنصر اصلی که با کربن ترکیبات آلی را تشکیل می دهند، هیدروژن می باشد. در گذشته به موادی که ریشه گیاهی یا حیوانی داشتند، مواد آلی می گفتند اما امروزه مواد آلی را می توان از طریق روش های صنعتی و آزمایشگاهی و به کمک مواد معدنی نیز سنتز کرد. موادی که از منابع آلی بدست می آیند، در یک ویژگی مشترک هستند و آن اشتراک در دارا بودن عنصر کربن است. دو منبع بزرگ مواد آلی که از آنها مواد آلی با ترکیبات ساده، تأمین می شوند، نفت و زغال سنگ هستند، این دو ماده فسیلی در مفهوم قدیمی آلی بوده و حاصل تجزیه جانوران و گیاهان هستند. این ترکیبات ساده به عنوان مصالح ساختمانی، در ساختن ترکیبات بزرگتر و پیچیده تر مصرف می گردند. شیمی آلی، شیمی ترکیبات کربن با سایر عناصر به ویژه هیدروژن، اکسیژن، نیتروژن، هالوژن ها و غیر فلزات دیگر نظیر گوگرد و منیزیوم است. الکل ها، اترها، هیدروکربن ها، آلدئیدها، کتون ها، کربوکسیلیک اسیدها، ترکیبات آلیفاتیک حلقوی، کربانیون ها، آمین ها، فنل ها، درشت مولکول ها و بسپارها (پلیمر) و نظیر آنها جزء مواد آلی بوده و مباحث شیمی آلی را به خود اختصاص داده اند. امروزه از مواد آلی و دانش شیمی آلی در رنگ سازی، کاغذ و جوهرسازی، مواد غذایی، پوشاک، پتروشیمی، مواد پلاستیکی و لاستیکی، داروسازی، پزشکی و ده ها صنعت دیگر بهره می برند. افزون بر بیست میلیون ترکیب شناخته شده کربن وجود دارد و هر ساله نیم میلیون ملکول جدید به خانواده مواد آلی اضافه می شوند. شیمی آلی شالوده زیست شناسی و پزشکی است. ساختمان موجودات زنده به غیر از آب، عمدتا” از مواد آلی ساخته شده اند، مولکول های مورد بحث در زیست شناسی مولکولی همان مولکول های آلی هستند. امروزه ما در عصر کربن زندگی می کنیم، هر روزه روزنامه ها و مجلات، ذهن ما را متوجه ترکیبات کربن نظیر کلسترول، چربی های اشباع نشده، هورمون ها، استروئیدها، حشره کش ها و فرومون ها می نماید. در دهه های گذشته به خاطر نفت جنگ های متعددی راه افتاده است، همچنین دو فاجعه نازک شدن لایه اوزون که عمدتا” به خاطر وجود کلرو فلوئورو کربن ها می باشد و پدیده گازهای گلخانه ای که ناشی از حضور متان، کلرو فلوئورو کربن ها و دی اکسید کربن است، زندگی انسان ها را به خطر انداخته است.

آرایش و درشتی مولکول های مواد آلی
تا حدود سال ۱۸۵۰ میلادی بسیاری از دانشمندان بر این باور بودند که منشأ مواد آلی، جانداران و گیاهان هستند، آنها تصور می کردند که مواد آلی را هرگز نمی توان از مواد معدنی و غیر آلی تولید نمود. دانشمندان همواره دنبال پاسخ به این پرسش بودند که چه ویژگی در ترکیبات کربن وجود دارد که آنها را از ترکیبات مربوط به صد و چند عنصر دیگر جدول تناوبی متمایز کرده است. تعداد بسیاری از ترکیبات کربن وجود دارند که مولکول های آنها می توانند بسیار بزرگ و پیچیده باشند. تعداد ترکیباتی که دارای عنصر کربن هستند چندین برابر بیشتر از تعداد ترکیبات بدون کربن است. مولکول های آلی شامل هزاران اتم شناخته شده اند و ترتیب قرار گرفتن اتم ها حتی در مولکول های نسبتا” کوچک نیز بسیار پیچیده است. یکی از مسائل اصلی در شیمی آلی، آگاهی از طرز قرار گرفتن اتم ها در مولکول ها و یا تعیین ساختمان ترکیبات است.
ویژگی منحصر به فرد اتم کربن
اتم های کربن می توانند به میزانی که برای اتم هیچ عنصر دیگری مقدور نیست، به یکدیگر متصل شوند. همچنین اتم های کربن می توانند زنجیرهایی شامل هزاران اتم و یا حلقه هایی با اندازه های متفاوت ایجاد نمایند، زنجیرها و حلقه ها می توانند دارای شاخه و پیوندهای عرضی باشند، به اتم های کربن این زنجیرها و حلقه ها، اتم های دیگری نیز می تواند وصل شود، این اتم ها معمولا” هیدروژن، فلوئور، کلر، برم، ید، اکسیژن، نیتروژن، گوگرد، فسفر و سایر اتم های مختلف می باشند. هر آرایش مختلف از اتم ها مربوط به ترکیب متفاوتی است و هر ترکیب یک سری خواص شیمیایی و فیزیکی خاص خود را دارد، از این رو غیر منتظره نیست که امروزه ده ها میلیون ترکیب شناخته شده کربن وجود داشته باشد.
پیوند شیمیایی
بررسی ساختمان مولکول ها را باید با بحث درباره پیوندهای شیمیایی یعنی نیروهایی که اتم ها را در یک مولکول نگاه می دارند، شروع نمود. دو نوع پیوند یونی و کووالانسی، پیوندهایی هستند که به وسیله آن اتم ها با یکدیگر اتصال برقرار می کنند. از میان این دو پیوند، پیوند کووالانسی، پیوند متدوال در ترکیبات کربن است و مهمترین پیوند در مطالعه شیمی آلی است.
مواد آلی در شیمی آلی
مواد آلی دارای گستره ای بزرگ می باشند و بسیار متفاوت و متنوع هستند. از این دسته مواد می توان، پارافین ها، روغن ها، هیدرو کربن ها، الفین ها، استیلن ها، ترپن ها، الکل ها، اسیدهای کربوکسیلیک، استرها، اترها، اپوکسیدها، آلدئیدها، کتون ها، آمین ها، آمیدها، ترکیبات آروماتیک، اسیدهای آلی، ایزوسیونات ها، محصولات استخلافی بنزن، الیاف نساجی، رنگ های رنگرزی و صنعتی و … را نام برد.
ترکیبات هیدرو کربنی
برخی از ترکیبات آلی فقط شامل دو عنصر، هیدروژن و کربن هستند و از این رو به عنوان هیدرو کربن شناخته می شوند. هیدرو کربن ها بر اساس ساختمان شان، به دو دسته اصلی، آلیفاتیک و آروماتیک تقسیم می شوند. هیدرو کربن های آلیفاتیک خود به گروه های آلکان ها، آلکن ها، آلکین ها و ترکیبات حلقه ای مشابه سیکلو آلکان ها و غیره تقسیم می گردند.
متان
ساده ترین ماده شیمی آلی متان است، مولکول متان دارای یک اتم مرکزی کربن و چهار اتم محیطی هیدروژن است که با زاویه ۱۰۹/۵ درجه دور اتم کربن قرار گرفته اند. متان محصول نهایی متلاشی شدن ناهوازی (بدون هوا) گیاهان یعنی از هم پاشیدگی بعضی از مولکول های پیچیده می باشد. متان تشکیل دهنده قسمت اعظم (حدود ۹۷ درصد) گاز طبیعی است. متان گاز آتشگیر خطرناک معادن زغال سنگ است و به صورت حباب های گاز از سطح مرداب ها خارج می گردد. گاز متان از ترکیب مونو اکسید کربن و هیدروژن حاصل می گردد.
کلرو فلوئورو کربن ها
مشتقات هالوژنه متان را کلرو فلوئورو کربن ها می گویند. اگر به جای هیدروژن های متان اتم های هالوژن جایگزین گردد، این محصولات حاصل می شوند. گازهای مورد استفاده در یخچال ها و کولرهای گازی و انواع اسپری، از این دسته مواد هستند. از جمله این مواد می توان به دی کلرو دی فلوئورو متان و کلرو تری فلوئورو متان اشاره کرد.
CF2Cl2 یا CFC12 دی کلرو دی فلوئورو متان
CF3Cl یا CFC11 کلرو تری فلوئورو متان
آلکان ها
آلکان ها که نقطه آغازگر آن ها متان است به ترکیبات غیر حلقوی و خطی کربن و هیدروژن اطلاق می شود، پیوند یگانه کووالانسی در این ترکیبات اتم های کربن و هیدروژن را به هم وصل کرده است. این هیدرو کربن ها بر اساس ساختمانشان به خانواده متان تعلق دارند و خواص آنها از خواص متان پیروی می کند. در آلکان ها تعداد اتم های هیدروژن نسبت به اتم های کربن، دو برابر به علاوه دو می باشد. یعنی مثلا” در مولکول بوتان، چهار اتم کربن و ده اتم هیدروژن وجود دارد. در آلکان ها، انتظار می رود هرچه تعداد اتم ها افزایش یابد، تعداد آرایش های ممکن اتم ها نیز زیادتر می شود. به تدریج که در سری آلکان ها پیش می رویم، تعداد ایزومرها در همرده های متوالی به میزان شگفت آوری افزایش می یابند. برای مثال هپتان دارای نه ایزومر می باشد، یعنی در شیمی آلی نه ماده مختلف با خواص متفاوت هستند که همگی فرمولشان C7H16 است. برای نامیدن ترکیبات مختلف و پیچیده آلی از روش استاندارد آیوپاک استفاده می کنند.
منابع
کتب شیمی آلی
شیمی آلی، جلد اول نوشتهٔ موریسون و بوید، ترجمهٔ علی پور جوادی
شیمی آلی، جلد دوم نوشتهٔ موریسون و بوید، ترجمهٔ علی پور جوادی
شیمی آلی، نوشتهٔ گراهام ت. سولومونز، ترجمهٔ سلاجقه، هروی و عبدی اسکویی
شیمی آلی، ویژگی ها و ترکیبات
شیمی آلی، ویژگی ها و ترکیبات
شیمی آلی زیر مجموعه ای از دانش شیمی است که درباره ترکیبات کربن یا مواد آلی سخن میگوید، عنصر اصلی که با کربن ترکیبات آلی را تشکیل می دهند، هیدروژن می باشد. در گذشته به موادی که ریشه گیاهی یا حیوانی داشتند، مواد آلی می گفتند اما امروزه مواد آلی را می توان از طریق روش های صنعتی و آزمایشگاهی و به کمک مواد معدنی نیز سنتز کرد. موادی که از منابع آلی بدست می آیند، در یک ویژگی مشترک هستند و آن اشتراک در دارا بودن عنصر کربن است. دو منبع بزرگ مواد آلی که از آنها مواد آلی با ترکیبات ساده، تأمین می شوند، نفت و زغال سنگ هستند، این دو ماده فسیلی در مفهوم قدیمی آلی بوده و حاصل تجزیه جانوران و گیاهان هستند. این ترکیبات ساده به عنوان مصالح ساختمانی، در ساختن ترکیبات بزرگتر و پیچیده تر مصرف می گردند. شیمی آلی، شیمی ترکیبات کربن با سایر عناصر به ویژه هیدروژن، اکسیژن، نیتروژن، هالوژن ها و غیر فلزات دیگر نظیر گوگرد و منیزیوم است. الکل ها، اترها، هیدروکربن ها، آلدئیدها، کتون ها، کربوکسیلیک اسیدها، ترکیبات آلیفاتیک حلقوی، کربانیون ها، آمین ها، فنل ها، درشت مولکول ها و بسپارها (پلیمر) و نظیر آنها جزء مواد آلی بوده و مباحث شیمی آلی را به خود اختصاص داده اند. امروزه از مواد آلی و دانش شیمی آلی در رنگ سازی، کاغذ و جوهرسازی، مواد غذایی، پوشاک، پتروشیمی، مواد پلاستیکی و لاستیکی، داروسازی، پزشکی و ده ها صنعت دیگر بهره می برند. افزون بر بیست میلیون ترکیب شناخته شده کربن وجود دارد و هر ساله نیم میلیون ملکول جدید به خانواده مواد آلی اضافه می شوند. شیمی آلی شالوده زیست شناسی و پزشکی است. ساختمان موجودات زنده به غیر از آب، عمدتا” از مواد آلی ساخته شده اند، مولکول های مورد بحث در زیست شناسی مولکولی همان مولکول های آلی هستند. امروزه ما در عصر کربن زندگی می کنیم، هر روزه روزنامه ها و مجلات، ذهن ما را متوجه ترکیبات کربن نظیر کلسترول، چربی های اشباع نشده، هورمون ها، استروئیدها، حشره کش ها و فرومون ها می نماید. در دهه های گذشته به خاطر نفت جنگ های متعددی راه افتاده است، همچنین دو فاجعه نازک شدن لایه اوزون که عمدتا” به خاطر وجود کلرو فلوئورو کربن ها می باشد و پدیده گازهای گلخانه ای که ناشی از حضور متان، کلرو فلوئورو کربن ها و دی اکسید کربن است، زندگی انسان ها را به خطر انداخته است.

آرایش و درشتی مولکول های مواد آلی
تا حدود سال ۱۸۵۰ میلادی بسیاری از دانشمندان بر این باور بودند که منشأ مواد آلی، جانداران و گیاهان هستند، آنها تصور می کردند که مواد آلی را هرگز نمی توان از مواد معدنی و غیر آلی تولید نمود. دانشمندان همواره دنبال پاسخ به این پرسش بودند که چه ویژگی در ترکیبات کربن وجود دارد که آنها را از ترکیبات مربوط به صد و چند عنصر دیگر جدول تناوبی متمایز کرده است. تعداد بسیاری از ترکیبات کربن وجود دارند که مولکول های آنها می توانند بسیار بزرگ و پیچیده باشند. تعداد ترکیباتی که دارای عنصر کربن هستند چندین برابر بیشتر از تعداد ترکیبات بدون کربن است. مولکول های آلی شامل هزاران اتم شناخته شده اند و ترتیب قرار گرفتن اتم ها حتی در مولکول های نسبتا” کوچک نیز بسیار پیچیده است. یکی از مسائل اصلی در شیمی آلی، آگاهی از طرز قرار گرفتن اتم ها در مولکول ها و یا تعیین ساختمان ترکیبات است.
ویژگی منحصر به فرد اتم کربن
اتم های کربن می توانند به میزانی که برای اتم هیچ عنصر دیگری مقدور نیست، به یکدیگر متصل شوند. همچنین اتم های کربن می توانند زنجیرهایی شامل هزاران اتم و یا حلقه هایی با اندازه های متفاوت ایجاد نمایند، زنجیرها و حلقه ها می توانند دارای شاخه و پیوندهای عرضی باشند، به اتم های کربن این زنجیرها و حلقه ها، اتم های دیگری نیز می تواند وصل شود، این اتم ها معمولا” هیدروژن، فلوئور، کلر، برم، ید، اکسیژن، نیتروژن، گوگرد، فسفر و سایر اتم های مختلف می باشند. هر آرایش مختلف از اتم ها مربوط به ترکیب متفاوتی است و هر ترکیب یک سری خواص شیمیایی و فیزیکی خاص خود را دارد، از این رو غیر منتظره نیست که امروزه ده ها میلیون ترکیب شناخته شده کربن وجود داشته باشد.
پیوند شیمیایی
بررسی ساختمان مولکول ها را باید با بحث درباره پیوندهای شیمیایی یعنی نیروهایی که اتم ها را در یک مولکول نگاه می دارند، شروع نمود. دو نوع پیوند یونی و کووالانسی، پیوندهایی هستند که به وسیله آن اتم ها با یکدیگر اتصال برقرار می کنند. از میان این دو پیوند، پیوند کووالانسی، پیوند متدوال در ترکیبات کربن است و مهمترین پیوند در مطالعه شیمی آلی است.
مواد آلی در شیمی آلی
مواد آلی دارای گستره ای بزرگ می باشند و بسیار متفاوت و متنوع هستند. از این دسته مواد می توان، پارافین ها، روغن ها، هیدرو کربن ها، الفین ها، استیلن ها، ترپن ها، الکل ها، اسیدهای کربوکسیلیک، استرها، اترها، اپوکسیدها، آلدئیدها، کتون ها، آمین ها، آمیدها، ترکیبات آروماتیک، اسیدهای آلی، ایزوسیونات ها، محصولات استخلافی بنزن، الیاف نساجی، رنگ های رنگرزی و صنعتی و … را نام برد.
ترکیبات هیدرو کربنی
برخی از ترکیبات آلی فقط شامل دو عنصر، هیدروژن و کربن هستند و از این رو به عنوان هیدرو کربن شناخته می شوند. هیدرو کربن ها بر اساس ساختمان شان، به دو دسته اصلی، آلیفاتیک و آروماتیک تقسیم می شوند. هیدرو کربن های آلیفاتیک خود به گروه های آلکان ها، آلکن ها، آلکین ها و ترکیبات حلقه ای مشابه سیکلو آلکان ها و غیره تقسیم می گردند.
متان
ساده ترین ماده شیمی آلی متان است، مولکول متان دارای یک اتم مرکزی کربن و چهار اتم محیطی هیدروژن است که با زاویه ۱۰۹/۵ درجه دور اتم کربن قرار گرفته اند. متان محصول نهایی متلاشی شدن ناهوازی (بدون هوا) گیاهان یعنی از هم پاشیدگی بعضی از مولکول های پیچیده می باشد. متان تشکیل دهنده قسمت اعظم (حدود ۹۷ درصد) گاز طبیعی است. متان گاز آتشگیر خطرناک معادن زغال سنگ است و به صورت حباب های گاز از سطح مرداب ها خارج می گردد. گاز متان از ترکیب مونو اکسید کربن و هیدروژن حاصل می گردد.
کلرو فلوئورو کربن ها
مشتقات هالوژنه متان را کلرو فلوئورو کربن ها می گویند. اگر به جای هیدروژن های متان اتم های هالوژن جایگزین گردد، این محصولات حاصل می شوند. گازهای مورد استفاده در یخچال ها و کولرهای گازی و انواع اسپری، از این دسته مواد هستند. از جمله این مواد می توان به دی کلرو دی فلوئورو متان و کلرو تری فلوئورو متان اشاره کرد.
CF2Cl2 یا CFC12 دی کلرو دی فلوئورو متان
CF3Cl یا CFC11 کلرو تری فلوئورو متان
آلکان ها
آلکان ها که نقطه آغازگر آن ها متان است به ترکیبات غیر حلقوی و خطی کربن و هیدروژن اطلاق می شود، پیوند یگانه کووالانسی در این ترکیبات اتم های کربن و هیدروژن را به هم وصل کرده است. این هیدرو کربن ها بر اساس ساختمانشان به خانواده متان تعلق دارند و خواص آنها از خواص متان پیروی می کند. در آلکان ها تعداد اتم های هیدروژن نسبت به اتم های کربن، دو برابر به علاوه دو می باشد. یعنی مثلا” در مولکول بوتان، چهار اتم کربن و ده اتم هیدروژن وجود دارد. در آلکان ها، انتظار می رود هرچه تعداد اتم ها افزایش یابد، تعداد آرایش های ممکن اتم ها نیز زیادتر می شود. به تدریج که در سری آلکان ها پیش می رویم، تعداد ایزومرها در همرده های متوالی به میزان شگفت آوری افزایش می یابند. برای مثال هپتان دارای نه ایزومر می باشد، یعنی در شیمی آلی نه ماده مختلف با خواص متفاوت هستند که همگی فرمولشان C7H16 است. برای نامیدن ترکیبات مختلف و پیچیده آلی از روش استاندارد آیوپاک استفاده می کنند.
منابع
کتب شیمی آلی
شیمی آلی، جلد اول نوشتهٔ موریسون و بوید، ترجمهٔ علی پور جوادی
شیمی آلی، جلد دوم نوشتهٔ موریسون و بوید، ترجمهٔ علی پور جوادی
شیمی آلی، نوشتهٔ گراهام ت. سولومونز، ترجمهٔ سلاجقه، هروی و عبدی اسکویی
شیمی آلی فلزی
شیمی آلی فلزی
شیمی آلی فلزی (Organometallic Chemistry)، شیمی ترکیباتی است که حداقل یک پیوند کربن _ فلز داشته (C-M) و شامل فلزات واقعی و شبه فلزات از قبیل Si ، As ، B و فلزات واسطه باشند. بنابراین این پیوند میتواند یک پیوند کووالانسی ساده باشد. مانند پیوند در تترااتیل سرب. یا یک پیوند داتیو باشد، مانند پیوند در فروسن یا حتی یونی باشد، مانند پیوند در اتیل سدیم.
خواص ترکیبات آلی فلزی
شباهت ترکیبات آلی فلزی از نظر خواص فیزیکی به ترکیبات آلی در مقایسه با ترکیبات معدنی بیشتر است. بسیاری از این ترکیبات دارای ساختار مولکولی منفک هستند و در نتیجه در دماهای معمولی بصورت بلورهایی با نقطه ذوب پایین، مایعات و یا گازها دیده میشوند. این ترکیبات معمولاً در حلالهای آلی کم قطبی از قبیل تولوئن، اترها و یا دیکلرو متان قابل حل هستند.
از نظر خصوصیات شیمیایی، تفاوت قابل ملاحظهای بین ترکیبات آلی فلزی وجود دارد و مثلا، پایداری حرارتی آنها بطور قابل ملاحظهای به ترکیب شیمیایی آنها بستگی دارد. از این رو، تترامتیل سیلان پس از چندین روز نگهداری در دمای ۵۰۰ درجه سانتیگراد بلا تغییر میماند، در حالی که تترامتیل تیتان در دمای اتاق سریعا تجزیه میشود.
پایداری در برابر اکسایش
کلیه ترکیبات آلی فلزی از نقطه نظر ترمودینامیکی اکسایش ناپایدار هستند. نیروی محرکه لازم برای اکسایش این ترکیبات به واسطه تشکیل اکسید فلز، دیاکسید کربن و آب که انرژی آزاد منفی بالایی دارند، تامین میشود. همچنین بیشتر این ترکیبات از نقطه نظر سینتیکی در دمای اتاق یا پایینتر در مقابل اکسایش ناپایدار هستند. اغلب این ترکیبات مانند دی متیل روی، تری متیل قلع، تری متیل ایندیوم به خودی خود در هوا آتش میگیرند. همچنین بیشتر مشتقات فلزات واسطه در برابر اکسیژن حساس هستند و معمولاً متداول و غالبا ضروری است که این مشتقات، زیر اتمسفر بیاثری از گاز نیتروژن یا آرگون مورد بررسی و مطالعه قرار بگیرند.
پایداری در برابر آبکافت
سرعت آبکافت یک ترکیب آلی فلزی به قطبیت پیوند C-M آن بستگی دارد. مثلا وقتی قطبیت پیوند زیاد باشد (مثلا در تری متیل آلومنیوم ) حمله مولکولهای آب بطور سریع انجام میگیرد، در صورتی که تری متیل بور در دمای اتاق با وجود داشتن یک اوربیتال خالی ۲P در اتم بور تحت تاثیر مولکولهای آب قرار نمیگیرد. اکثر مشتقات آلی فلزات واسطه خنثی در مقابل فرآیند آبکافت بی اثر هستند، ولی لانتانیدهای آلی بشدت، مستعد آبکافت میباشند و علت آن را میتوان به خاصیت قطبی پیوند، اندازه بزرگتر اتم مرکزی و حضور تعداد زیاد اوربیتالهای خالی کم انرژی نسبت داد.
مشتقات عناصر واسطه
در مورد فلزات واسطه (که برای تشکیل پیوند از اوربیتالها و الکترونهای d و در صورت لزوم f استفاده میکنند) معمولاً کمپلکسهای π دارنده پیوندهای داتیو تشکیل میشود. به عبارت دیگر، عناصر واسطه d اغلب نه تنها دارای پیوندهای سیگما بوده، بلکه پیوندهایی از نوع π نیز دارند. به عبارت سادهتر، پیوند بین اتمهای واسطه و مولکولهای آلی اشباع نشده بوسیله تبادل الکترون در دو جهت مخالف تشکیل میشود.
سادهترین مثال پیوندی است که بین مونوکسید کربن و اتم فلز در کربونیلهای فلزی تشکیل میشود. در این گونه پیوندها فلز باید اوربیتالهای خالی d داشته باشد، تا بتواند الکترونهای داده شده توسط CO را بپذیرد و نیز باید اوربیتالهای اشغال شده d داشته باشد، تا بتواند الکترونهای خود در اوربیتال d را به لیگاند بدهد.
برخی از کاربردهای ترکیبات آلی فلزی
استفاده از ترکیبات آلی سیلسیم به عنوان واسطه در تهیه پلیمرهای سیلسیم (سیلیکونها).
استفاده از آلومینیوم آلکینها به عنوان کاتالیزور در پلیمر کردن و الیگومر کردن اولفینها در مقیاس وسیع.
استفاده از تترااتیل سرب و تترامتیل سرب برای بالا بردن درجه اکتان بنزین.
استفاده از مشتقات آلی فلزات واسطه در داروسازی در سطح گسترده
استفاده از ترکیبات آلی ایریدیوم و روتنیوم در مقابله با مقاومت دارویی
استفاده از ترکیبات آلی قلع به عنوان آفت کش و پایدار کننده پلیمرها.
کربونیل دار کردن متانول جهت تولید اسید استیک، از اسید استیک در تهیه پلی وینیل استات و محصول آبکافت آن یعنی پلی وینیل الکل، استفاده میگردد و همچنین در تهیه انیدرید استیک که مورد نیاز صنایع تولید کننده الیاف استات سلولز و پلاستیکها میباشد، کاربرد دارد و نیز در تهیه استرهای استات که یکی از حلالهای صنعتی مهم به شمار میرود، از اسید استیک استفاده میشود.
کاربرد طیف سنجی HECTOR در رزونانس مغناطیسی هستهای
کاربرد طیف سنجی HECTOR در رزونانس مغناطیسی هستهای

اطلاعات اولیه
اتمهای پروتون و کربن به دو طریق بسیار مهم با یکدیگر بر همکنش مینمایند. اول اینکه آن دو ، دارای خواص مغناطیسی هستند و هر کدام قادرند موجب القای آسایش بر دیگری گردند. دوم اینکه دو نوع هسته مزبور میتوانند با یکدیگر کوپلاژ اسپینی انجام دهند. این بر همکنش میتواند بسیار سودمند باشد، چون پروتونها و کربنهایی که مستقیما به یکدیگر متصلند، دارای مقدار J ای بوده که حداقل ده برابر بیش از کوپلاژهای دو پیوندی و سه پیوندی بین هستهها هستند. این اختلاف شاخص در میزان کوپلاژها برای ما یک طریقه حساس شناسایی کربنها و پروتونهایی را فراهم میآورد که مستقیما به یکدیگر متصل هستند.
برای به دست آوردن ارتباط بین کربنها و پروتونهای چسبیده در یک آزمایش دو بعدی ، ما باید قادر به ترسیم تغییر مکان شیمیایی اتمهای C13 بر روی یک محور و تغییرات مکان شیمیایی و پروتونها بر روی محور دیگر باشیم. نقطه ای از شدت در این نوع طیف دو بعدی ، وجود یک پیوند C-H را مشخص میسازد. آزمایش ارتباط تغییر مکان شیمیایی ناهم هسته (HETCOR) برای فراهم ساختن طیف مورد پسند طراحی شده است.
مروری بر آزمایش HETCOR
میخواهیم اجازه دهیم بردارهای مغناطیس شدن پروتونها با سرعتهای متفاوتی که بوسیله تغییرات مکان شیمیایی آنها دیکته شدهاند، حرکت تقدیمی کنند. لذا ، یک تپ ˚۹۰ را به پروتونها اعمال مینماییم و سپس ، یک زمان تکامل ، (t1) را وارد میکنیم. این تپ ، بردار مغناطیس شدن توده را به صفحه X´Y´ منحرف میسازد. طی دوره تکامل ، اسپینهای پروتون با سرعتی که از روی تغییرات مکان شیمیایی و کوپلاژهای آنان با دیگر هستهها (هم پروتونها و هم کربنها) تعیین میگردد، حرکت تقدیمی میکنند.
پروتونهایی که به اتمهای C13 متصل هستند، نهتنها تغییرات مکان شیمیایی خود را خلال t1 تجزیه میکنند، بلکه کوپلاژهای اسپین همهسته و ناهمهسته با اتمهای C13 چسبیده را نیز تجربه مینمایند. این بر همکنش C13 و H1 است که ارتباط مورد علاقه ما را برقرار میسازد. پس از زمان تکامل ، بطور همزمان ، تپهای ˚۹۰ را به پروتونها و کربنها اعمال میکنیم. این تپها باعث انتقال مغناطیس شدن از پروتونها به کربنها میگردد. چون در خلال t 1 مغناطیس شدن کربن بوسیله فرکانسهای تقدیمی پروتون نشاندار میشود، لذا سیگنالهای C13 که در طی مدت t2 شناسایی شدهاند، بوسیله تغییرات مکان شیمیایی پروتونهای جفت شده تعدیل میشوند. آنگاه ، مغناطیس شدن C13 در t2 شناسایی شده تا یک کربن بخصوص را که حامل هر نوع تعدیل پروتون است، شناسایی کند.

تشریح HECTOR
آزمایش HETCOR همچون تمامی آزمایشهای دو بعدی ، محیط هستهها را در خلال t1 تشریح مینماید. بدلیل طریقه ای که در آن ، توالی تپ HETCOR ساخته شده، تنها بر همکنشهایی که مسوول تعدیل کنندگی حالات اسپینی پروتون هستند، تغییرات مکان شیمیایی پروتون و کوپلاژهای هم هستهاند. هر اتم C13 ممکن است دارای یک یا چند قله ظاهر شونده بر روی محور f2 باشد که مربوط به تغییر مکان شیمیایی آن است.
تعدیل تغییر مکان شیمیایی پروتون موجب میگردد تا شدت سیگنال پروتون دو بعدی در مقدار f1 ای ظاهر گردد که مربوط به تغییر مکان شیمیایی پروتون است. تعدیلهای بیشتر پروتون با فرکانس بسیار کوچکتر از کوپلاژهای هم هسته (H-H) ناشی میشوند. این تعدیلها ، ساختمان ظریفی را بر روی قلل در راستای محور f1 فراهم میکنند. میتوانیم این ساختمان ظریف را دقیقا همان گونه که در طیف عادی پروتون انجام میدادیم، تفسیر کنیم، اما در این مورد در مییابیم که مقدار تغییر مکان شیمیایی پروتون ، به پروتونی تعلق دارد که به یک هسته C13 ویژه چسبیده است که آن کربن در مقدار تغییر مکان شیمیایی مربوط به خود ظاهر میگردد.
پس میتوان اتمهای کربن را بر اساس تغییران مکان شیمیایی معلوم پروتون گمارش نمود یا میتوان پروتونها را بر پایه تغییرات مکان شیمیایی معلوم کربن گمارش کرد. برای مثال ، ممکن است یک طیف پروتون شلوغ ، ولی طیف کربن (همان ترکیب) با درجه تفکیک خوب داشته باشیم (یا بر عکس) این روش بویژه آزمایش HETCOR را در تفسیر طیفهای مولکولهای بزرگ و پیچیده مفید میسازد. یک فن حتی قدرتمندتر ، استفاده از نتایج حاصل از هر د و آزمایش COPY و HETCOR است.
اندازه گیری نقطه ی ذوب ترکیبات آلی
اندازه گیری نقطه ی ذوب ترکیبات آلی
هدف: برای دو هدف مختلف می توان از آن استفاده کرد ۱_ شناسایی ۲_ تعیین خلوص ترکیبات آلی .
وقتی ماده ناشناخته است مهمترین کار: تعیین ثابت های فیزیکی (خصوصیت های فیزیکی) ترکیب آلی است ؛ مهمترین ثابت های فیزیکی عبارتند از :
رنگ ماده، بو، شکل بلور ها، نقطه ی ذوب، نقطه ی جوش، نقطه ی تصعید، ضریب انکسار نور، طیفIR ، طیف NMR، طیفUV، طیف سنجی جرمی، آنالیز عنصری .
در اثر وجود ناخالصی رنگ بلور ها تغییر می کند ، شکل بلور ها هم این گونه است .
نقطه ی ذوب: دمای نقطه ای را به ما می دهد که در آن از فاز جامد به مایع می رویم به شرطی که در انتقال از جامد به مایع در فشار استاندارد محیط با ۱ اتمسفر صورت بگیرد .
تعریف دوم و صحیح تر : عبارت از دمایی است که در آن دما فاز جامد و مایع به حالت تعادل می رسد .
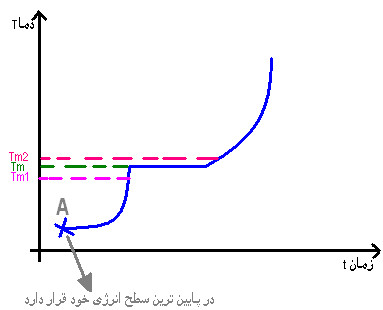
توضیح شکل : فرض می کنیم ۱۰۰ تا مولکول A داریم، به محض افزایش دمابه لحظه ای خواهیم رسید که نیرو های جاذبه ی بین مولکولی A بر همدیگر غلبه کرده و ماده ی جامد از شبکه ی کریستالی خود خارج می شود واتم ها روی همدیگر میلغزندو ما ده از حالت جامد وارد حالت مایع خواهد شد .Tm نقطه ی ذوب A در آن حالت جامد و مایع A برابر خواهند بود و تعادل برقرار خواهد شد بین جامد و مایع ، Tm1 نقطه ی ذوب ابتدایی A هنوز تعادل برقرار نشده است ، Tm2 نقطه ی نهایی تمامی ماده به مایع تبدیل شده است .
قابل توجه است که رطوبت نیز مانند ناخالصی عمل کرده و در خصوصیت های فیزیکی ماده تغییر ایجاد می کند .
ناخالصی ها دو ماهیت دارند که یا محلول اند یا نامحلول، ناخالصی محلول روی نقطه ی ذوب تاثیر منفی خواهد داشت چون میزان محلول را زیاد می کند در صورتی که اگر ناخالصی نامحلول باشد با افزایش دما نمی تواند وارد فاز مایع شود بنابر این هیچ تاثیری نمی گذارد.
مثال :سولفات کلسیم در نقطه ی ذوب استانلید تاثیر نمی گذارد،
کلرور سدیم در فاز مایع است و در نقطهی ذوب استانلید تاثیر می گذارد .
بنابراین: آن موادی به عنوان ناخالصی محلول عمل می کنند که یک خاصیت یونیزاسیون در آن ها وجود داشته باشد.
رطوبت تاثیر منفی می گذارد .
برای یک ماده ی خالص حداکثر اختلاف دمایی که بین Tm1 و Tm2 خواهیم دید بین ۰٫۵ تا ۱ درجه خواهد بود اما برای ماده ای که ناخالصی دارد این اختلاف دما بین ۵ تا ۱۰ درجه می تواند باشد و هر چه ناخالصی بیشتر باشد اختلاف دما بین نقطه ی ذوب ابتدایی و انتهایی بیشتر خواهد بود .
نحوه ی تشخیص نقطه ی ذوب: اگر ماده جمع شود ( کم شود ) و یا گاهی شبنم مانند هایی در محلول ایجاد می شود که همیشه نشان دهنده ی نقطه ی ذئب ابتدایی است ، اگر محلول شفاف شد به نقطه ی ذوب نهایی رسیده ایم و همه ی جامد ها به مایع تبدیل شده است .
اندازه گیری نقطه ی ذوب مخلوط چند ماده :
اتکتیک: نقطه یذوب چند ترکیب که باهم ترکیب شده اند.
فرض کنید دو ماده داریم :A با نقطه ی ذئب ۱۱۸ درجه و B با نقطه ی ذوب ۹۰ درجه وقتی آنها را با هم مخلوط می کنیم دو امکان وجود دارد:۱_ تشکیل مخلوط اتکتیک می دهند : نقطه ی ذوب حاصل خیلی پایین تر از مواد اولیه است مثلا ۶۰ درجه ۲_ تشکیل مخلوط اتکتیک نمی دهند : در این صورت B به صورت ناخالصی روی A عمل می کند و نقطه ی ذوب A را حداکثر ۲۰ درجه کم میکند مثلا مخلوط حاصل دارای نقطه ی ذوبی برابر ۱۰۸ درجه خواهد شد .
شاخصه ی نقطه ی اتکتیک این است که نقطه ی ذوب مخلوط حاصل بسیار پایین تر از نقطه ی ذوب مواد اولیه است.
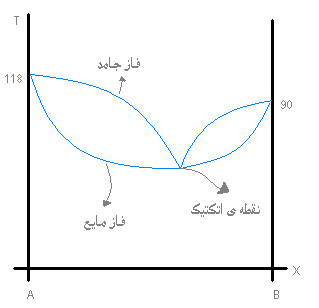
نکته : در این نقطه فاز جامد A و B را داریم که با مایع های خود در تعادل اند(شباهتی با نقطه ی ذوب دارد) .
از نقطه ی اتکتیک در صنعت برای تهیه ی آلیاژ های مختلف استفاده می شود بدین صورت که دو فلز را ذوب می کنند و اگر آن دو به یک نقطه ی اتکتیک رسیدند بنابر این می توان از آن ها آلیاژ تهیه کرد.
آلیاژها: ترکیبی از چند فلز با نسبت های مختلف که در تهیه ی آن ها از نقطه ی اتکتیک استفاده می شود.
نقطه ی اتکتیک فقط در مورد فلزات نیست در بعضی مواقع مواد آلی در کنار آب (رطوبت ) نقطه ی اتکتیک تشکیل داده و نقطه ی ذوب بسیار پایین خواهد آمد .
اندازه گیری نقطه ی ذوب در آزمایشگاه ها با استفاده از لوله ی مویین است .
سوالات مطرح :
چه عواملی در نقطه ی ذوب تاثیر می گذارد ؟ شکل بلور ها ، اندازه ی بلور ها، مقدار بلور ها، فشرده بودن بلور ها.
چرا در نزدیکی Tm1 باید دما را کنترل کنیم ؟ باید کنترل کنیم تا بتوانیم نقطه ی ذوب را اندازه گیری کنیم.
منبع : سایت علمی نخبگان جوان
تاثیر ارتعاش کششی C=C در طیف سنجی مادون قرمز
تاثیر ارتعاش کششی C=C در طیف سنجی مادون قرمز
طیف مادون قرمز برای هر ماده ای در محدوده خاصی قرار دارد. ولی در یک مولکول ، استخلافهای موجود ، محدوده طیف را تحت تاثیر قرار میدهند. میخواهیم تاثیر ارتعاش کششی C=C را بر طیف سنجی مادون قرمز بررسی کنیم.
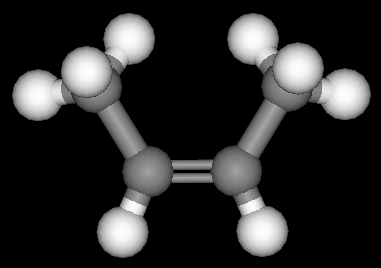
آلکن های آلکیل استخلاف شده ساده
فرکانس کششی برای آلکن های غیر حلقوی ساده ، معمولا بین ۱۶۴۰ و ۱۶۷۰سانتیمتر به توان ۱- ظاهر میشود. تعدد گروههای آلکیلی بر روی پیوند دو گانه ، فرکانسهای C=C را افزایش میدهد. برای مثال ، آلکن های تک استخلافی ساده دارای مقادیر حدود ۱۶۴۰سانتیمتر به توان ۱- هستند، آلکنهای ۱،۱- دو استخلافی در حدود ۱۶۵۰ سانتی متر به توان ۱- جذب میکنند و آلکن های سه و چهار استخلافی در نزدیکی ۱۶۷۰ سانتیمتر به توان ۱- جذب میدهند.
آلکن های ترانس – دو استخلافی در فرکانسهای بالاتری (۱۶۷۰ سانتیمتر به توان ۱- ) نسبت به آلکن های سیس- دو استخلافی (۱۶۵۸ سانتیمتر به توان ۱- ) جذب میدهند. متاسفانه گروه C=C دارای شدت نسبتا ضعیف است که قطعا بمراتب ضعیفتر از گروه C=O است. در بسیاری از موارد همچون آلکن های چهار استخلافی ، پیوند دو گانه ممکن است آنقدر ضعیف باشد که دیده نشود. اگر گروههای متصل بطور متقارن چیده شده باشند، تغییری در گشتاور دو قطبی در حین ارتعاش کششی رخ نداده ، لذا ، هیچ گونه جذب مادون قرمز مشاهده نمیگردد.
سیس – آلکن ها که کممتقارنتر از ترانس – آلکن ها هستند، عموما شدیدتر از مورد دوم جذب میکنند. پیوندهای دو گانه موجود در حلقهها (چون غالبا متقارن هستند) ضعیفتر از آنهایی که در حلقه نیستند، جذب صورت میدهند. پیوندهای دو گانه انتهایی در آلکن های تک استخلافی معمولا جذب قویتری دارند.
اثر مزدوج شدن
مزدوج شدن یک پیوند دو گانه C=C با یک گروه کربونیل یا پیوند دو گانه C=C دیگر ، خصلت پیوند ساده را در پیوند چند گانه بیشتر کرده ( از طریق رزونانس ) و این امر باعث کاهش ثابت نیرو K و بنابراین کاهش فرکانس ارتعاشی میگردد. بهعنوان مثال ، پیوند دوگانه وینیل در استایرن جذبی در ۱۶۳۰ سانتیمتر به توان ۱- میدهد. هرگاه چندین پیوند دو گانه وجود داشته باشد، از روی تعداد جذبهای C=C میتوان به تعداد پیوندهای دو گانه مزدوج پی برد. مثالی در این مورد ۱و۳- پنتان دیاِن است که جذبهای آن را در ۱۶۰۰ و ۱۶۵۰ سانتیمتر به توان ۱- میتوان یافت.
استثنایی که در این قاعده وجود دارد، بوتا دیاِن است که تنها یک نوار نزدیک ۱۶۰۰سانتیمتر به توان ۱- میدهد. اگر پیوند دو گانه با یک گروه کربونیل مزدوج شود، شدت جذب آن معمولا قدری توسط خاصیت دو قطبی قوی گروه کربونیل افزایش مییابد.
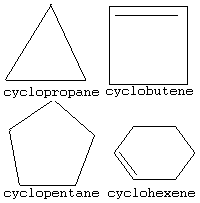
اثر اندازه حلقه در حلقههای حاوی پیوندهای دو گانه درونی
فرکانس جذب پیوندهای دو گانه داخلی در ترکیبات حلقوی به اندازه حلقه بسیار حساس است. با کاهش زاویه داخلی و میل آن به مینیمم مقدار ˚۹۰ در سیکلوبوتن ، فرکانس جذب نیز کاهش مییابد. فرکانس جذب هنگامی که زاویه به ˚۶۰ در سیکلوپروپن برسد، مجددا افزایش مییابد. این افزایش غیرمنتظره فرکانس ، بدین دلیل رخ میدهد که ارتعاش C=C در سیکلوپروپن بشدت با ارتعاش پیوند ساده C-C مجاور ادغام میشود. هنگامی که پیوندهای C-C بر محور C=C عمود هستند (همان طور که در سیکلوبوتن است) ، نوع ارتعاش آنها بر ارتعاش پیوند C=C عمود است (روی محور دیگر) و دیگر این ارتعاشات ادغام نمیگردند.
هنگامی که زاویه بزرگتر از ˚۹۰ (˚۱۲۰ در مثال فوق) باشد، ارتعاش کششی پیوند ساده C-C به دو جزء تقسیم میگردد که یکی از آنها منطبق بر جهت ارتعاش کششی C=C است. در دیاگرام ، اجزاء b و a از بردار کششی C-C نشان داده شدهاند. چون که جزء a در جهت بردار کششی C=C قرار دارد، پیوندهای C=C و C-C ادغام گشته و باعث بالا رفتن فرکانس جذب میگردند. طرح مشابهی نیز برای سیکلوپروپن وجود دارد که دارای زاویه کوچکتر از ˚۹۰ است.
هنگامی که یک یا دو گروه آلکیلی مستقیما به پیوند دو گانه متصل باشند، افزایش قابل ملاحظه ای در فرکانس جذب یک پیوند دو گانه موجود در حلقه مشاهده میگردد. این افزایش برای حلقههای کوچک ، بویژه سیکلوپروپنها ، بسیار محسوس است. هنگامی که یک گروه آلکیل به پیوند دو گانه متصل گردد، مقدار پایه ۱۶۵۶ سانتیمتر به توان ۱- برای سیکلوپروپن به حدود ۱۷۸۸ سانتیمتر به توان ۱- افزایش مییابد؛ با وجود دو گروه آلکیل این مقدار به حدود ۱۸۸۳ سانتیمتر به توان ۱- فزونی مییابد.
فهم این نکته پُر اهمیت است که اندازه حلقه باید پیش از بکارگیری قواعد فوق تعیین گردد. برای مثال ، توجه کنید که پیوندهای دو گانه در ۱و۲- دی آلکیل سیکلوپنتن و ۱و۲- دی آلکیل سیکلوهگزن ، تقریبا در یک فرکانس جذب میدهند.
اثر اندازه حلقه در حلقه های حاوی پیوندیهای دو گانه خارجی
در پیوندهای دو گانه خارجی ، کاهش اندازه حلقه باعث افزایش فرکانس جذب میگردد. آلن نمونه بارزی از یک ترکیب دارای پیوند دو گانه خارجی است. حلقههای کوچکتر نیاز بیشتری به استفاده از خصلت p در سااخت پیوندهای C-C دارند تا جوابگوی نیاز زوایای کوچک باشند. این مساله باعث از میان برداشته شدن خصلت p از پیوند سیگمای پیوند دو گانه شده ، ولی در عوض به آن خصلت s بیشتری میدهد؛ بنابراین قدرت و استحکام پیوند دو گانه افزایش مییابد. پس ثابت نیروی K افزایش یافته و فرکانس جذب نیز فزونی میگیرد.
آسپارتام
آسپارتام aspartame
مشهورترین شیرین کننده ی مصنوعی که در رستورانها ، سوپرمارکت ها وحتی آشپزخانه ی شما یافت می شود آسپارتام است که تحت نام های تجاری نوتراسوئیت ، اکوال و آمینوسوئیت به فروش می رسد.
درحقیقت شما به ندرت می توانید یک بسته آدامس یا شیرینی بدون آسپارتام پیدا کنید .
در اکثر رستورانها کنار پاکت های حاوی شکر یک پاکت حاوی ماده شیمیایی آسپارتام است. آسپارتام ازنظر سم شناسی excitotoin-1 است (یک فرآیند پاتولوژیکی است که در آن سلولهای عصبی به دلیل تحریکات زیاد نوروترانسمیتورهایی نظیر گلوتامیت تخریب شده و میمیرند).
علیرغم خطرات مصرف آسپارتام شرکت های سازنده از تأثیرات جانبی مصرف آن صرف نظر کرده و مرتباً به تبلیغ آن می پردازند.
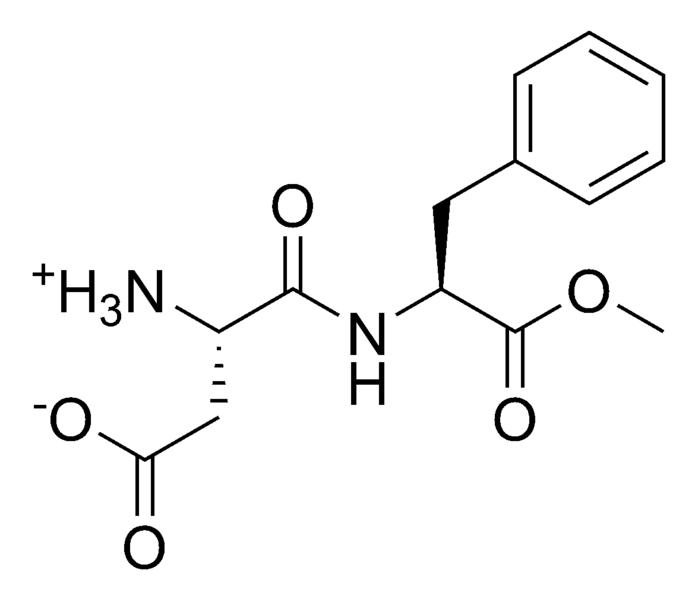
آسپارتام چیست؟
آسپارتام یک ترکیب سنتتیک است که از اتصال دو اسید آمینه ی فنیل آلانین و اسید آسپارتیک با یک متیل الکل بوجود می آید ، متیل الکل در بدن به اسید فورمیک (سم موجود در نیش مورچه) و فورمالدئید ( مایع مورد استفاده در مومیایی ) شکسته می شود. هر بار که نوشیدنیها یا آدامس های حاوی آسپارتام را مصرف می کنید بدن شما مقداری از این مواد ناسالم را دریافت می کند.
اسیدهای آمینه مستقیماً به مغز وارد شده و سبب تغییر عملکرد سیستم عصبی شما می شوند . مغز شما به طور طبیعی از فنیل آلانین استفاده می کند اما با مصرف آسپارتام شما مقدار بیشتری فنیل آلانین به مغز می رسانید.
تحقیقات نشان می دهد که افزایش مقدار فنیل آلانین در مغز سبب افزایش حملات ناگهانی غش (seizure) می شود مواد شیمیایی دیگر متیل الکل ، فورمیک اسید و فورمالدئید – نیز مواد بسیار سمی هستند که با خوردن آسپارتام وارد بدن شما می شود . بهر حال MSG(مونوسدیم گلوتامات) که یک اکسایتوتوکسین دیگر است به صورت همزمان با آسپارتام عمل کرده وسبب ایجاد تخریب بیشتر می شود.
واکنش ها و مضرات جانبی آسپارتام
از سال ۱۹۸۰ دپارتمان سلامت خدمات انسانی آمریکا بیش از ۱۰ هزار شکایت از واکنش های مضر آسپارتام دریافت کرده است. اگر چه قدرت اقتصادی بزرگی که در خفای فروش آسپارتام وجود دارد از فاش کردن این مضرات جلوگیری می کند.
تعدادی از مضرات جانبی شایع مصرف آسپارتام عبارتند از:
عوارض عصبی: تشنج، سردرد، میگرن، سرگیجه شدید، لرزش، ضعف حافظه ، خواب آلودگی ، بی حسی دست و پا، اختلال در تکلم، بیش فعالی، خستگی شدید پاها، دردهای صورت، رعشه ،اختلال عدم توجه و تومرهای مغزی.
عوارض چشمی و گوش: نابینایی ، کاهش بینایی وتاری دید، ایجاد برق های نورانی در چشم ، کاهش دید شب، درد در چشمان ، بیرون زدگی چشم ها ازحدقه ،ایجاد صداهایی شبیه به زنگ یا سوت در گوش، از دست رفتن شنوایی.
عوارض روانی: افسردگی ، حساسیت و زود رنجی، پرخاشگری، اضطراب ، تغییرات شخصیتی ، بی خوابی، فوبیا.
عوارض قلبی: افزایش ضربان قلب، تنگی تنفس، افزایش فشار خون.
عوارض گوارشی: حالت تهوع، اسهال، درد شکمی.
عوارض آلرژیک : تنفس همراه با صدا، آسم، خارش و رش پوستی
آسپارتام و دیابت
آسپارتام به خصوص برای افراد دیابتی بسیار خطرناک است زیرا سبب بدتر شدن وضعیت قند خون شده ، از سوی دیگر سبب بروز تشنج می شود و با انسولین واکنش عکس می دهد. آسپارتام سبب وخیم شدن وضعیت رتینوپاتی دیابتی، تخریب عصب بینایی و منجربه کوری می شود.متیل الکل آزاد شده از مصرف آسپارتام سبب نوروپاتی و افزایش خطر قطع عضو در افراد دیابتی می شود.
آسپارتام وکاهش وزن
بسیاری از افراد به جای داشتن برنامه ی غذایی سالم و انجام ورزش به مصرف غذاهای فاقد قند که حاوی شیرین کننده هایی نظیر آسپارتام هستند،استفاده می کنند. متاسفانه آسپارتام میل به خوردن مواد شیرین را افزایش می دهد و اشتها را زیادتر کرده و سبب افزایش وزن می شود.
چنانچه تابحال از آسپارتام استفاده می کردید حال باید چه کنید؟
اولین قدم قطع مصرف آن است، حتی مصرف مقادیر کم آن نیز موجب مسمومیت بدن شما می شود. در خرید اقلام غذایی خود دقت کنید که در آن آسپارتام نبا شد، بهتر است از شیرین کننده ی گیاهی استویا استفاده کنید. این ماده در آمریکای جنوبی به مدت چهارصد سال بدون بروز هیچ عارضه ای استفاده شده است و ۲۰ بار از شکر شیرین تر است بنابراین مقدار بسیار کم آن می تواند شیرینی زیادی را ایجاد کند.
برای فعال کردن سیستم سم زدایی بدن یعنی کبد بهتر است از ساپلمینت های خاصی برای فعال تر کردن این سیستم استفاده کنید.
از مواد گیاهی نظیر Indole-3 Carbinol که در سبزیجات چلیپایی نظیر کلم بروکلی، کلم برگ، جوانه ی Brassel و گل کلم وجود دارد، استفاده کنید. از گیاه خار مریم یا Milk thistle یا silymarin که سم زدایی کبد را افزایش می دهد، استفاده کنید.
از زردچوبه که حاوی Curcumin(ماده ی زرد رنگ) است به عنوان ماده ی آنتی اکسیدان و سم زدا بیشتر استفاده کنید.
از ویتامینهای C و گروه E ,B و منیزیوم و سلنیوم استفاده کنید، زیرا به فرایند سم زادیی کمک می کنند . بیاد داشته باشید سلامت شما وابسته به چیزی است که می خورید.
استیک اسید
استیک اسید
اسید استیک جز اسیدهای کربوکسیلیک میباشد و در نامگذاری آیوپاک به اسید اتانوئیک معروف است. این اسید دارای فرمول شیمیایی میباشد و در قسمت چشایی طعم ترشی، شبیه طعم سرکه میدهد.
این اسید یک اسید ضعیف بوده زیرا تنها مقداری اسید جدا شده در محلول آبی می باشد. استیک اسید بدون آب و خالص (استیک اسید یخی) یک مایع بدون رنگ بوده که آب را از محیط اطرافش جذب میکند(هیگروسکوپی) و در دمای ۱۶٫۵ C(62 F) به شکل یک جامد کریستالی بی رنگ منجمد می شود. اسید خالص و محلول های غلیظ آن بسیار خورنده هستند.
استیک اسید یکی از ساده ترین کربکسیلیک اسید ها است. این اسید یک معرف شیمیایی مهم بوده و یک ماده شیمیایی صنعتی مورد استفاده در تولید مواد زیر است: پلی اتیلن ترفتالات که به صورت عمده در بطری های نوشابه استفاده می شود؛ سلولوز استات که به طور عمده در فیلم عکاسی استفاده می شود؛ پلی وینیل استات برای چسب چوب به علاوه فایبر ها و فابریک های مصنوعی. در خانه، استیک اسید رقیق برای باز کردن لوله ها استفاده می شود. در صنعت غذا، استیک اسید تحت کد افزودنی E260 به عنوان تنظیم اسیدی و به عنوان چاشنی استفاده می شود.
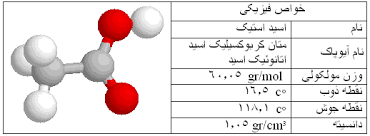
تقاضای جهانی استیک اسید در حدود ۶٫۵ میلیون تون در سال (Mt/a) که حدود ۱٫۵ Mt/a از طریق بازیافت برآورده می شود. باقی آن توسط بازار خوراک پتروشیمیایی یا منابع بیولوژیکی تولید می شود. استیک اسید رقیق تولید شده توسط تخمیر طبیعی، سرکه نامیده می شود.
باکتریهای مخمر سرکه به دلیل تمایل به تولید اسید استیک به این نام معروف شدهاند. این باکتریها در مواد غذایی، آب و خاک یافت میشوند. اسید استیک بطور طبیعی از میوهها و برخی مواد غذایی فاسد شده از فرایند تخمیر تولید میشوند و از قدیمیترین ترکیبات شیمیایی شناخته شده توسط انسان میباشد.
نام «اسید استیک» رایجترین و رسمیترین نامی است که توسط IUPAC برای این ماده بکار میرود. این نام از کلمه لاتین acetum، به معنی سرکه، گرفته شدهاست. «اسید اتانوئیک» که به عنوان مترادف آن بکار میرود، یک نام سازمانیافتهاست که گاهی در معرفی نامگذاری مواد شیمیایی عنوان میشود.
«اسید استیک منجمد» یک نام سطحی برای اسید استیک بدون آب است. مثل نام آلمانی Eisessig(که به صورت تحتالطفظی به معنای سرکه یخی است)، این نام، از نام کریستالهایی برگرفته شده که در دمای اندکی زیر ۷/۱۶ درجه سانتیگراد (حدود ۶۲ درجه فارنهایت) شکل میگیرند.
رایجترین و رسمیترین نام اختصاری برای اسید استیک AcOH یا HOAc است که در آن Ac مخفف گروه عاملی|گروه استیل است CH۳−C(=O)−؛ در واکنشهای اسیدی، علامت اختصاری HAc بکار میرود که در آن Ac مخفف استات آنیون (CH۳COO−) میباشد، هر چند که بسیاری این نامگذاری را گمراه کننده میدانند. باید توجه داشت که در حالتی دیگر نباید Ac را با مخفف عنصر شیمیایی اکتینیم اشتباه گرفت.
فرمول ساده اسید استیک CH۲O و فرمولی مولکولی آن C۲H۴O۲ است. حالت آخر با هدف نشان دادن بهتر ساختار، بصورت CH۳-COOH, CH۳COOH، یا CH۳CO۲H نوشته میشود. یونی که در نتیجه حذف پروتون (H+) از اسید استیک به جا میماند «استات» آنیون نام دارد. همچنین نام «استات» به نمکی که حاوی این آنیون یا یک استر اسید استیک باشد اطلاق میگردد.
اسید استیک مایع، مانند آب و اتانول یک حلال پروتوندار آبدوست (مولکول قطبی|قطبی) است. این ماده با ثابت دی الکتریک ۲/۶، میتواند علاوه بر حل کردن ترکیبات قطبی همچون نمکهای معدنی و شکرها، ترکیبات غیر قطبی همچون روغنها و عناصر شیمیایی مثل سولفور و آیودین را در خود حل کند. این ماده با بسیاری از حلالهای قطبی و غیر قطبی همچون آب، کلروفورم و هگزان مخلوط میشود. این خاصیت انحلال و امتزاجپذیری اسید استیک آنرا به یک ماده شیمیایی پرکاربرد صنعتی تبدیل کردهاست.
اسید استیک، هم بطور مصنوعی و هم از طریق تخمیر باکتریایی، تولید میشود. امروزه روش باکتریایی تنها ۱۰ درصد از تولید را به خود اختصاص دادهاست اما به دلیل اینکه قوانین جهانی مربوط به سلامت غذا بر تهیه سرکه خوراکی از مواد بیولوژیکی تاکید میکند، این روش همچنان برای تولید سرکه استفاده میشود. تقریبا حدود ۷۵ درصد از اسید استیک تولید شده برای استفادههای صنعتی، از کربندار کردن متانول و به روشی که در زیر میآید تولید میشود. برای بقیه مصارف، از روشهای دیگر استفاده میشود.[۷]
کل تولید جهانی اسید استیک ۵ میلیون تن در سال برآورد میشود که نیمی از آن درایالات متحده تولید میشود. تولید این ماده در اروپا ۱ میلیون تن در سال است که میزان آن رو به کاهش نهاده؛ در ژاپن نیز تولید این ماده ۷/۰ میلیون تن در سال است. از سوی دیگر هرسالانه ۵/۱ میلیون تن اسید استیک بازیافت میشود که تولید جهانی را به ۵/۶ میلیون تن در سال میرساند.
بزرگترین تولیدکنندگان اسید استیک دست نخورده، سلانس و بیپی ،صنایع شیمیایی بی پی هستند. از دیگر تولیدکنندگان عمده این ماده میتوان به ملنیوم کمیکالز، استرلینگ کمیکالز، سام سونگ، ایستمن و سوونسک اتانول کمی اشاره کرد.
اسید استیک غلیظ خورندهاست و در نتیجه باید با احتیاط با آن کار کرد، زیرا باعث سوختگی، آسیبهای دائم چشمی و سوزش اعضای دارای مایعات مخاطی میشود. این تاولها و آبلهها ممکن است تا چند ساعت پس از در معرض قرار گرفتن پدیدار نشوند. به هنگام کار کردن با این ترکیبها باید از دستکشهای مقاوم از جنس پلاستیک نیتریل استفاده کرد چراکه استفاده ازدستکشهای لاتکس از ایمنی لازم برخوردار نیست. اسید استیک غلیظ در شرایط آزمایشگاهی به سختی مشتعل میشود. با بالا رفتن دما از مرز ۳۹ درجه سانتیگراد، ریسک تبدیل شدن آن به یک ماده منفجره در مجاورت هوا افزایش مییابد. (حد انفجار: ۴/۵ درصد تا ۱۶ درصد).
خطر محلولهای اسید استیک به میزان غلظت آن بستگی دارد. محلولهایی که اسید استیک آنها بیش از ۲۵ درصد است، به خاطر بوی زننده و بخار خورنده آنها در هود بخار نگهداری میشود. اسید استیک رقیق به شکل سرکه بی ضرر است. با اینحال وارد کردن محلولهای قویتر در آن، برای انسان و حیوانات ضرر دارد. این محلول به سیستم گوارش آسیب زده و تغییری مهلک را در خاصیت اسیدی خون ایجاد میکند.
به دلیل عدم تطبیق آن، پیشنهاد می شود که اسید استیک را از اسید کرومیک و اتیلن گلایکول و اسید نیتریک و اسید پر کلریک و پرمنگنات ها و پر اکسید ها و هیدروکسیل ها دور نگه دارید.
استیک اسید
استیک اسید
اسید استیک جز اسیدهای کربوکسیلیک میباشد و در نامگذاری آیوپاک به اسید اتانوئیک معروف است. این اسید دارای فرمول شیمیایی میباشد و در قسمت چشایی طعم ترشی، شبیه طعم سرکه میدهد.
این اسید یک اسید ضعیف بوده زیرا تنها مقداری اسید جدا شده در محلول آبی می باشد. استیک اسید بدون آب و خالص (استیک اسید یخی) یک مایع بدون رنگ بوده که آب را از محیط اطرافش جذب میکند(هیگروسکوپی) و در دمای ۱۶٫۵ C(62 F) به شکل یک جامد کریستالی بی رنگ منجمد می شود. اسید خالص و محلول های غلیظ آن بسیار خورنده هستند.
استیک اسید یکی از ساده ترین کربکسیلیک اسید ها است. این اسید یک معرف شیمیایی مهم بوده و یک ماده شیمیایی صنعتی مورد استفاده در تولید مواد زیر است: پلی اتیلن ترفتالات که به صورت عمده در بطری های نوشابه استفاده می شود؛ سلولوز استات که به طور عمده در فیلم عکاسی استفاده می شود؛ پلی وینیل استات برای چسب چوب به علاوه فایبر ها و فابریک های مصنوعی. در خانه، استیک اسید رقیق برای باز کردن لوله ها استفاده می شود. در صنعت غذا، استیک اسید تحت کد افزودنی E260 به عنوان تنظیم اسیدی و به عنوان چاشنی استفاده می شود.

تقاضای جهانی استیک اسید در حدود ۶٫۵ میلیون تون در سال (Mt/a) که حدود ۱٫۵ Mt/a از طریق بازیافت برآورده می شود. باقی آن توسط بازار خوراک پتروشیمیایی یا منابع بیولوژیکی تولید می شود. استیک اسید رقیق تولید شده توسط تخمیر طبیعی، سرکه نامیده می شود.
باکتریهای مخمر سرکه به دلیل تمایل به تولید اسید استیک به این نام معروف شدهاند. این باکتریها در مواد غذایی، آب و خاک یافت میشوند. اسید استیک بطور طبیعی از میوهها و برخی مواد غذایی فاسد شده از فرایند تخمیر تولید میشوند و از قدیمیترین ترکیبات شیمیایی شناخته شده توسط انسان میباشد.
نام «اسید استیک» رایجترین و رسمیترین نامی است که توسط IUPAC برای این ماده بکار میرود. این نام از کلمه لاتین acetum، به معنی سرکه، گرفته شدهاست. «اسید اتانوئیک» که به عنوان مترادف آن بکار میرود، یک نام سازمانیافتهاست که گاهی در معرفی نامگذاری مواد شیمیایی عنوان میشود.
«اسید استیک منجمد» یک نام سطحی برای اسید استیک بدون آب است. مثل نام آلمانی Eisessig(که به صورت تحتالطفظی به معنای سرکه یخی است)، این نام، از نام کریستالهایی برگرفته شده که در دمای اندکی زیر ۷/۱۶ درجه سانتیگراد (حدود ۶۲ درجه فارنهایت) شکل میگیرند.
رایجترین و رسمیترین نام اختصاری برای اسید استیک AcOH یا HOAc است که در آن Ac مخفف گروه عاملی|گروه استیل است CH۳−C(=O)−؛ در واکنشهای اسیدی، علامت اختصاری HAc بکار میرود که در آن Ac مخفف استات آنیون (CH۳COO−) میباشد، هر چند که بسیاری این نامگذاری را گمراه کننده میدانند. باید توجه داشت که در حالتی دیگر نباید Ac را با مخفف عنصر شیمیایی اکتینیم اشتباه گرفت.
فرمول ساده اسید استیک CH۲O و فرمولی مولکولی آن C۲H۴O۲ است. حالت آخر با هدف نشان دادن بهتر ساختار، بصورت CH۳-COOH, CH۳COOH، یا CH۳CO۲H نوشته میشود. یونی که در نتیجه حذف پروتون (H+) از اسید استیک به جا میماند «استات» آنیون نام دارد. همچنین نام «استات» به نمکی که حاوی این آنیون یا یک استر اسید استیک باشد اطلاق میگردد.
اسید استیک مایع، مانند آب و اتانول یک حلال پروتوندار آبدوست (مولکول قطبی|قطبی) است. این ماده با ثابت دی الکتریک ۲/۶، میتواند علاوه بر حل کردن ترکیبات قطبی همچون نمکهای معدنی و شکرها، ترکیبات غیر قطبی همچون روغنها و عناصر شیمیایی مثل سولفور و آیودین را در خود حل کند. این ماده با بسیاری از حلالهای قطبی و غیر قطبی همچون آب، کلروفورم و هگزان مخلوط میشود. این خاصیت انحلال و امتزاجپذیری اسید استیک آنرا به یک ماده شیمیایی پرکاربرد صنعتی تبدیل کردهاست.
اسید استیک، هم بطور مصنوعی و هم از طریق تخمیر باکتریایی، تولید میشود. امروزه روش باکتریایی تنها ۱۰ درصد از تولید را به خود اختصاص دادهاست اما به دلیل اینکه قوانین جهانی مربوط به سلامت غذا بر تهیه سرکه خوراکی از مواد بیولوژیکی تاکید میکند، این روش همچنان برای تولید سرکه استفاده میشود. تقریبا حدود ۷۵ درصد از اسید استیک تولید شده برای استفادههای صنعتی، از کربندار کردن متانول و به روشی که در زیر میآید تولید میشود. برای بقیه مصارف، از روشهای دیگر استفاده میشود.[۷]
کل تولید جهانی اسید استیک ۵ میلیون تن در سال برآورد میشود که نیمی از آن درایالات متحده تولید میشود. تولید این ماده در اروپا ۱ میلیون تن در سال است که میزان آن رو به کاهش نهاده؛ در ژاپن نیز تولید این ماده ۷/۰ میلیون تن در سال است. از سوی دیگر هرسالانه ۵/۱ میلیون تن اسید استیک بازیافت میشود که تولید جهانی را به ۵/۶ میلیون تن در سال میرساند.
بزرگترین تولیدکنندگان اسید استیک دست نخورده، سلانس و بیپی ،صنایع شیمیایی بی پی هستند. از دیگر تولیدکنندگان عمده این ماده میتوان به ملنیوم کمیکالز، استرلینگ کمیکالز، سام سونگ، ایستمن و سوونسک اتانول کمی اشاره کرد.
اسید استیک غلیظ خورندهاست و در نتیجه باید با احتیاط با آن کار کرد، زیرا باعث سوختگی، آسیبهای دائم چشمی و سوزش اعضای دارای مایعات مخاطی میشود. این تاولها و آبلهها ممکن است تا چند ساعت پس از در معرض قرار گرفتن پدیدار نشوند. به هنگام کار کردن با این ترکیبها باید از دستکشهای مقاوم از جنس پلاستیک نیتریل استفاده کرد چراکه استفاده ازدستکشهای لاتکس از ایمنی لازم برخوردار نیست. اسید استیک غلیظ در شرایط آزمایشگاهی به سختی مشتعل میشود. با بالا رفتن دما از مرز ۳۹ درجه سانتیگراد، ریسک تبدیل شدن آن به یک ماده منفجره در مجاورت هوا افزایش مییابد. (حد انفجار: ۴/۵ درصد تا ۱۶ درصد).
خطر محلولهای اسید استیک به میزان غلظت آن بستگی دارد. محلولهایی که اسید استیک آنها بیش از ۲۵ درصد است، به خاطر بوی زننده و بخار خورنده آنها در هود بخار نگهداری میشود. اسید استیک رقیق به شکل سرکه بی ضرر است. با اینحال وارد کردن محلولهای قویتر در آن، برای انسان و حیوانات ضرر دارد. این محلول به سیستم گوارش آسیب زده و تغییری مهلک را در خاصیت اسیدی خون ایجاد میکند.
به دلیل عدم تطبیق آن، پیشنهاد می شود که اسید استیک را از اسید کرومیک و اتیلن گلایکول و اسید نیتریک و اسید پر کلریک و پرمنگنات ها و پر اکسید ها و هیدروکسیل ها دور نگه دارید.
استیک اسید
استیک اسید
اسید استیک جز اسیدهای کربوکسیلیک میباشد و در نامگذاری آیوپاک به اسید اتانوئیک معروف است. این اسید دارای فرمول شیمیایی میباشد و در قسمت چشایی طعم ترشی، شبیه طعم سرکه میدهد.
این اسید یک اسید ضعیف بوده زیرا تنها مقداری اسید جدا شده در محلول آبی می باشد. استیک اسید بدون آب و خالص (استیک اسید یخی) یک مایع بدون رنگ بوده که آب را از محیط اطرافش جذب میکند(هیگروسکوپی) و در دمای ۱۶٫۵ C(62 F) به شکل یک جامد کریستالی بی رنگ منجمد می شود. اسید خالص و محلول های غلیظ آن بسیار خورنده هستند.
استیک اسید یکی از ساده ترین کربکسیلیک اسید ها است. این اسید یک معرف شیمیایی مهم بوده و یک ماده شیمیایی صنعتی مورد استفاده در تولید مواد زیر است: پلی اتیلن ترفتالات که به صورت عمده در بطری های نوشابه استفاده می شود؛ سلولوز استات که به طور عمده در فیلم عکاسی استفاده می شود؛ پلی وینیل استات برای چسب چوب به علاوه فایبر ها و فابریک های مصنوعی. در خانه، استیک اسید رقیق برای باز کردن لوله ها استفاده می شود. در صنعت غذا، استیک اسید تحت کد افزودنی E260 به عنوان تنظیم اسیدی و به عنوان چاشنی استفاده می شود.

تقاضای جهانی استیک اسید در حدود ۶٫۵ میلیون تون در سال (Mt/a) که حدود ۱٫۵ Mt/a از طریق بازیافت برآورده می شود. باقی آن توسط بازار خوراک پتروشیمیایی یا منابع بیولوژیکی تولید می شود. استیک اسید رقیق تولید شده توسط تخمیر طبیعی، سرکه نامیده می شود.
باکتریهای مخمر سرکه به دلیل تمایل به تولید اسید استیک به این نام معروف شدهاند. این باکتریها در مواد غذایی، آب و خاک یافت میشوند. اسید استیک بطور طبیعی از میوهها و برخی مواد غذایی فاسد شده از فرایند تخمیر تولید میشوند و از قدیمیترین ترکیبات شیمیایی شناخته شده توسط انسان میباشد.
نام «اسید استیک» رایجترین و رسمیترین نامی است که توسط IUPAC برای این ماده بکار میرود. این نام از کلمه لاتین acetum، به معنی سرکه، گرفته شدهاست. «اسید اتانوئیک» که به عنوان مترادف آن بکار میرود، یک نام سازمانیافتهاست که گاهی در معرفی نامگذاری مواد شیمیایی عنوان میشود.
«اسید استیک منجمد» یک نام سطحی برای اسید استیک بدون آب است. مثل نام آلمانی Eisessig(که به صورت تحتالطفظی به معنای سرکه یخی است)، این نام، از نام کریستالهایی برگرفته شده که در دمای اندکی زیر ۷/۱۶ درجه سانتیگراد (حدود ۶۲ درجه فارنهایت) شکل میگیرند.
رایجترین و رسمیترین نام اختصاری برای اسید استیک AcOH یا HOAc است که در آن Ac مخفف گروه عاملی|گروه استیل است CH۳−C(=O)−؛ در واکنشهای اسیدی، علامت اختصاری HAc بکار میرود که در آن Ac مخفف استات آنیون (CH۳COO−) میباشد، هر چند که بسیاری این نامگذاری را گمراه کننده میدانند. باید توجه داشت که در حالتی دیگر نباید Ac را با مخفف عنصر شیمیایی اکتینیم اشتباه گرفت.
فرمول ساده اسید استیک CH۲O و فرمولی مولکولی آن C۲H۴O۲ است. حالت آخر با هدف نشان دادن بهتر ساختار، بصورت CH۳-COOH, CH۳COOH، یا CH۳CO۲H نوشته میشود. یونی که در نتیجه حذف پروتون (H+) از اسید استیک به جا میماند «استات» آنیون نام دارد. همچنین نام «استات» به نمکی که حاوی این آنیون یا یک استر اسید استیک باشد اطلاق میگردد.
اسید استیک مایع، مانند آب و اتانول یک حلال پروتوندار آبدوست (مولکول قطبی|قطبی) است. این ماده با ثابت دی الکتریک ۲/۶، میتواند علاوه بر حل کردن ترکیبات قطبی همچون نمکهای معدنی و شکرها، ترکیبات غیر قطبی همچون روغنها و عناصر شیمیایی مثل سولفور و آیودین را در خود حل کند. این ماده با بسیاری از حلالهای قطبی و غیر قطبی همچون آب، کلروفورم و هگزان مخلوط میشود. این خاصیت انحلال و امتزاجپذیری اسید استیک آنرا به یک ماده شیمیایی پرکاربرد صنعتی تبدیل کردهاست.
اسید استیک، هم بطور مصنوعی و هم از طریق تخمیر باکتریایی، تولید میشود. امروزه روش باکتریایی تنها ۱۰ درصد از تولید را به خود اختصاص دادهاست اما به دلیل اینکه قوانین جهانی مربوط به سلامت غذا بر تهیه سرکه خوراکی از مواد بیولوژیکی تاکید میکند، این روش همچنان برای تولید سرکه استفاده میشود. تقریبا حدود ۷۵ درصد از اسید استیک تولید شده برای استفادههای صنعتی، از کربندار کردن متانول و به روشی که در زیر میآید تولید میشود. برای بقیه مصارف، از روشهای دیگر استفاده میشود.[۷]
کل تولید جهانی اسید استیک ۵ میلیون تن در سال برآورد میشود که نیمی از آن درایالات متحده تولید میشود. تولید این ماده در اروپا ۱ میلیون تن در سال است که میزان آن رو به کاهش نهاده؛ در ژاپن نیز تولید این ماده ۷/۰ میلیون تن در سال است. از سوی دیگر هرسالانه ۵/۱ میلیون تن اسید استیک بازیافت میشود که تولید جهانی را به ۵/۶ میلیون تن در سال میرساند.
بزرگترین تولیدکنندگان اسید استیک دست نخورده، سلانس و بیپی ،صنایع شیمیایی بی پی هستند. از دیگر تولیدکنندگان عمده این ماده میتوان به ملنیوم کمیکالز، استرلینگ کمیکالز، سام سونگ، ایستمن و سوونسک اتانول کمی اشاره کرد.
اسید استیک غلیظ خورندهاست و در نتیجه باید با احتیاط با آن کار کرد، زیرا باعث سوختگی، آسیبهای دائم چشمی و سوزش اعضای دارای مایعات مخاطی میشود. این تاولها و آبلهها ممکن است تا چند ساعت پس از در معرض قرار گرفتن پدیدار نشوند. به هنگام کار کردن با این ترکیبها باید از دستکشهای مقاوم از جنس پلاستیک نیتریل استفاده کرد چراکه استفاده ازدستکشهای لاتکس از ایمنی لازم برخوردار نیست. اسید استیک غلیظ در شرایط آزمایشگاهی به سختی مشتعل میشود. با بالا رفتن دما از مرز ۳۹ درجه سانتیگراد، ریسک تبدیل شدن آن به یک ماده منفجره در مجاورت هوا افزایش مییابد. (حد انفجار: ۴/۵ درصد تا ۱۶ درصد).
خطر محلولهای اسید استیک به میزان غلظت آن بستگی دارد. محلولهایی که اسید استیک آنها بیش از ۲۵ درصد است، به خاطر بوی زننده و بخار خورنده آنها در هود بخار نگهداری میشود. اسید استیک رقیق به شکل سرکه بی ضرر است. با اینحال وارد کردن محلولهای قویتر در آن، برای انسان و حیوانات ضرر دارد. این محلول به سیستم گوارش آسیب زده و تغییری مهلک را در خاصیت اسیدی خون ایجاد میکند.
به دلیل عدم تطبیق آن، پیشنهاد می شود که اسید استیک را از اسید کرومیک و اتیلن گلایکول و اسید نیتریک و اسید پر کلریک و پرمنگنات ها و پر اکسید ها و هیدروکسیل ها دور نگه دارید.
شیمی آلی
شیمی آلی زیر مجموعه ای از دانش شیمی است که درباره ترکیبات کربن یا مواد آلی سخن میگوید، عنصر اصلی که با کربن ترکیبات آلی را تشکیل می دهند، هیدروژن می باشد. در گذشته به موادی که ریشه گیاهی یا حیوانی داشتند، مواد آلی می گفتند اما امروزه مواد آلی را می توان از طریق روش های صنعتی و آزمایشگاهی و به کمک مواد معدنی نیز سنتز کرد. موادی که از منابع آلی بدست می آیند، در یک ویژگی مشترک هستند و آن اشتراک در دارا بودن عنصر کربن است. دو منبع بزرگ مواد آلی که از آنها مواد آلی با ترکیبات ساده، تأمین می شوند، نفت و زغال سنگ هستند، این دو ماده فسیلی در مفهوم قدیمی آلی بوده و حاصل تجزیه جانوران و گیاهان هستند. این ترکیبات ساده به عنوان مصالح ساختمانی، در ساختن ترکیبات بزرگتر و پیچیده تر مصرف می گردند. شیمی آلی، شیمی ترکیبات کربن با سایر عناصر به ویژه هیدروژن، اکسیژن، نیتروژن، هالوژن ها و غیر فلزات دیگر نظیر گوگرد و منیزیوم است. الکل ها، اترها، هیدروکربن ها، آلدئیدها، کتون ها، کربوکسیلیک اسیدها، ترکیبات آلیفاتیک حلقوی، کربانیون ها، آمین ها، فنل ها، درشت مولکول ها و بسپارها (پلیمر) و نظیر آنها جزء مواد آلی بوده و مباحث شیمی آلی را به خود اختصاص داده اند. امروزه از مواد آلی و دانش شیمی آلی در رنگ سازی، کاغذ و جوهرسازی، مواد غذایی، پوشاک، پتروشیمی، مواد پلاستیکی و لاستیکی، داروسازی، پزشکی و ده ها صنعت دیگر بهره می برند. افزون بر بیست میلیون ترکیب شناخته شده کربن وجود دارد و هر ساله نیم میلیون ملکول جدید به خانواده مواد آلی اضافه می شوند. شیمی آلی شالوده زیست شناسی و پزشکی است. ساختمان موجودات زنده به غیر از آب، عمدتا” از مواد آلی ساخته شده اند، مولکول های مورد بحث در زیست شناسی مولکولی همان مولکول های آلی هستند. امروزه ما در عصر کربن زندگی می کنیم، هر روزه روزنامه ها و مجلات، ذهن ما را متوجه ترکیبات کربن نظیر کلسترول، چربی های اشباع نشده، هورمون ها، استروئیدها، حشره کش ها و فرومون ها می نماید. در دهه های گذشته به خاطر نفت جنگ های متعددی راه افتاده است، همچنین دو فاجعه نازک شدن لایه اوزون که عمدتا” به خاطر وجود کلرو فلوئورو کربن ها می باشد و پدیده گازهای گلخانه ای که ناشی از حضور متان، کلرو فلوئورو کربن ها و دی اکسید کربن است، زندگی انسان ها را به خطر انداخته است.
آرایش و درشتی مولکول های مواد آلی
تا حدود سال ۱۸۵۰ میلادی بسیاری از دانشمندان بر این باور بودند که منشأ مواد آلی، جانداران و گیاهان هستند، آنها تصور می کردند که مواد آلی را هرگز نمی توان از مواد معدنی و غیر آلی تولید نمود. دانشمندان همواره دنبال پاسخ به این پرسش بودند که چه ویژگی در ترکیبات کربن وجود دارد که آنها را از ترکیبات مربوط به صد و چند عنصر دیگر جدول تناوبی متمایز کرده است. تعداد بسیاری از ترکیبات کربن وجود دارند که مولکول های آنها می توانند بسیار بزرگ و پیچیده باشند. تعداد ترکیباتی که دارای عنصر کربن هستند چندین برابر بیشتر از تعداد ترکیبات بدون کربن است. مولکول های آلی شامل هزاران اتم شناخته شده اند و ترتیب قرار گرفتن اتم ها حتی در مولکول های نسبتا” کوچک نیز بسیار پیچیده است. یکی از مسائل اصلی در شیمی آلی، آگاهی از طرز قرار گرفتن اتم ها در مولکول ها و یا تعیین ساختمان ترکیبات است.
ویژگی منحصر به فرد اتم کربن
اتم های کربن می توانند به میزانی که برای اتم هیچ عنصر دیگری مقدور نیست، به یکدیگر متصل شوند. همچنین اتم های کربن می توانند زنجیرهایی شامل هزاران اتم و یا حلقه هایی با اندازه های متفاوت ایجاد نمایند، زنجیرها و حلقه ها می توانند دارای شاخه و پیوندهای عرضی باشند، به اتم های کربن این زنجیرها و حلقه ها، اتم های دیگری نیز می تواند وصل شود، این اتم ها معمولا” هیدروژن، فلوئور، کلر، برم، ید، اکسیژن، نیتروژن، گوگرد، فسفر و سایر اتم های مختلف می باشند. هر آرایش مختلف از اتم ها مربوط به ترکیب متفاوتی است و هر ترکیب یک سری خواص شیمیایی و فیزیکی خاص خود را دارد، از این رو غیر منتظره نیست که امروزه ده ها میلیون ترکیب شناخته شده کربن وجود داشته باشد.
پیوند شیمیایی
بررسی ساختمان مولکول ها را باید با بحث درباره پیوندهای شیمیایی یعنی نیروهایی که اتم ها را در یک مولکول نگاه می دارند، شروع نمود. دو نوع پیوند یونی و کووالانسی، پیوندهایی هستند که به وسیله آن اتم ها با یکدیگر اتصال برقرار می کنند. از میان این دو پیوند، پیوند کووالانسی، پیوند متدوال در ترکیبات کربن است و مهمترین پیوند در مطالعه شیمی آلی است.
مواد آلی در شیمی آلی
مواد آلی دارای گستره ای بزرگ می باشند و بسیار متفاوت و متنوع هستند. از این دسته مواد می توان، پارافین ها، روغن ها، هیدرو کربن ها، الفین ها، استیلن ها، ترپن ها، الکل ها، اسیدهای کربوکسیلیک، استرها، اترها، اپوکسیدها، آلدئیدها، کتون ها، آمین ها، آمیدها، ترکیبات آروماتیک، اسیدهای آلی، ایزوسیونات ها، محصولات استخلافی بنزن، الیاف نساجی، رنگ های رنگرزی و صنعتی و … را نام برد.
ترکیبات هیدرو کربنی
برخی از ترکیبات آلی فقط شامل دو عنصر، هیدروژن و کربن هستند و از این رو به عنوان هیدرو کربن شناخته می شوند. هیدرو کربن ها بر اساس ساختمان شان، به دو دسته اصلی، آلیفاتیک و آروماتیک تقسیم می شوند. هیدرو کربن های آلیفاتیک خود به گروه های آلکان ها، آلکن ها، آلکین ها و ترکیبات حلقه ای مشابه سیکلو آلکان ها و غیره تقسیم می گردند.
متان
ساده ترین ماده شیمی آلی متان است، مولکول متان دارای یک اتم مرکزی کربن و چهار اتم محیطی هیدروژن است که با زاویه ۱۰۹/۵ درجه دور اتم کربن قرار گرفته اند. متان محصول نهایی متلاشی شدن ناهوازی (بدون هوا) گیاهان یعنی از هم پاشیدگی بعضی از مولکول های پیچیده می باشد. متان تشکیل دهنده قسمت اعظم (حدود ۹۷ درصد) گاز طبیعی است. متان گاز آتشگیر خطرناک معادن زغال سنگ است و به صورت حباب های گاز از سطح مرداب ها خارج می گردد. گاز متان از ترکیب مونو اکسید کربن و هیدروژن حاصل می گردد.
کلرو فلوئورو کربن ها
مشتقات هالوژنه متان را کلرو فلوئورو کربن ها می گویند. اگر به جای هیدروژن های متان اتم های هالوژن جایگزین گردد، این محصولات حاصل می شوند. گازهای مورد استفاده در یخچال ها و کولرهای گازی و انواع اسپری، از این دسته مواد هستند. از جمله این مواد می توان به دی کلرو دی فلوئورو متان و کلرو تری فلوئورو متان اشاره کرد.
CF2Cl2 یا CFC12 دی کلرو دی فلوئورو متان
CF3Cl یا CFC11 کلرو تری فلوئورو متان
آلکان ها
آلکان ها که نقطه آغازگر آن ها متان است به ترکیبات غیر حلقوی و خطی کربن و هیدروژن اطلاق می شود، پیوند یگانه کووالانسی در این ترکیبات اتم های کربن و هیدروژن را به هم وصل کرده است. این هیدرو کربن ها بر اساس ساختمانشان به خانواده متان تعلق دارند و خواص آنها از خواص متان پیروی می کند. در آلکان ها تعداد اتم های هیدروژن نسبت به اتم های کربن، دو برابر به علاوه دو می باشد. یعنی مثلا” در مولکول بوتان، چهار اتم کربن و ده اتم هیدروژن وجود دارد. در آلکان ها، انتظار می رود هرچه تعداد اتم ها افزایش یابد، تعداد آرایش های ممکن اتم ها نیز زیادتر می شود. به تدریج که در سری آلکان ها پیش می رویم، تعداد ایزومرها در همرده های متوالی به میزان شگفت آوری افزایش می یابند. برای مثال هپتان دارای نه ایزومر می باشد، یعنی در شیمی آلی نه ماده مختلف با خواص متفاوت هستند که همگی فرمولشان C7H16 است. برای نامیدن ترکیبات مختلف و پیچیده آلی از روش استاندارد آیوپاک استفاده می کنند.
تهیه صابون با استفاده از چربیها
تهیه صابون با استفاده از چربیها
hز واکنش اسیدهای چرب منوکربوکسیلیک با گلیسیرین ، تولید گلیسیرید میگردد که نوع جامد را چربی و مایع را روغن مینامند. فرمول کلی اسیدهای چرب منوکربوکسیلیک را با RCOOH و گلیسیرین را نیز با فرمول تفسیری۳(C3H5(OH و واکنش آنها با هم ، تولید گلیسرید از اسید چرب میکند و گلیسیرین یک واکنش استری شدن است.
چربیها و روغنها در آب ، نامحلول اما در حلالهایی مانند بنزن ، نفت سفید ، دیسولفید کربن ، تترا کلرید کربن بخوبی حل میگردد. چربیها و روغنها در حرارتهای بالا ساختار آنها در هم ریخته و تولید ذرات کربن نموده که باعث ایجاد رنگ سیاه در مایع روغن یا چربی بکار رفته ، میشوند.
صابونها که به دو شکل مایع و جامد تهیه میشوند، نمکهای پتاسیم یا سدیم اسیدهای چرب منوکربوکسیلیک هستند. فرمول کلی صابون مایع R-COOK و صابون جامد R-COONa میباشد.
مواد و وسایل مورد نیاز
- راکتور یا ظرف انجام واکنش (واکنشگاه)
- منبع حرارت
- گلیسیرید یا چربی
- سود
شرح آزمایش
در یک ظرف (اگر مقدار مواد اولیه زیاد باشد، ظرف بزرگ) ، مقداری چربی ریخته و سود جامد و یا مایع را به آن اضافه میکنیم. واکنش هیدرولیز قلیایی انجام میشود و صابون و گلیسیرین به عنوان محصول جانبی حاصل میشود.
تخمیر
تخمیر پدیدهای است ناشی از مجموعه فعالیتهای زیستی که در آن ترکیبات آلی دارای مولکولهای بزرگ به ترکیبات دارای مولکولهای کوچکتر و سادهتر شکسته و تجزیه (کاتابولیسم) شده از فرآیند آن علاوه بر ایجاد ترکیبات آلی سادهتر، دیاکسیدکربن و انرژی نیز آزاد میگردد. با بیان دیگر تخمیر تجزیه ناقص بعضی از متابولیتها (ترکیبات آلی) به ترکیبات سادهتر همراه با انرژی توسط عامل تخمیری است.
نگاه کلی
در گیاهان تخمیر بیولوژیکی تنها تخمیر الکلی نبوده، ممکن است با کمی تخمیر لاکتیک نیز همراه باشد، برخی از سازوارههای حیاتی (میکروارگانیسمها) مانند قارچهای میکروسکوپی نیز قادر به تخمیرهایی مانند تخمیرهای سیتریک و اکسالیک روی قندهای شش کربنی (هگزوزها) و تخمیر استیک روی الکل اتیلیک و غیره هستند. باکتریها عامل انواع دیگری از تخمیر در طبیعت هستند. تخمیر بوتیریک سلولز لاشه برگها و تجزیه آنها که سبب افزایش ترکیبات آلی خاک میشود و همچنین تخمیرهای تعفنی مواد آلی توسط باکتریها صورت میگیرد.
تخمیر الکلی
پاستور اولین کسی است که نقش مخمرهای الکلی را نشان داد. بهترین مثال مخمرها، مخمرهای خمیرترش یا مخمر نانوایی است. اگر این مخمرها در محیط کشت گلوکز و در حضور اکسیژن کافی قرار گیرند، به شدت تقسیم شده، اکسیژن جذب کرده، دیاکسیدکربن آزاد میسازند. بیشترین سرعت واکنشهای ناشی از تنفس و شدت اکسیداسیون گلوکز این مخمرها که از گروه آسکومیست هستند هنگامی است که تنفس هوازی دارند اگر این مخمرها در داخل یک ظرف در بسته کشت داده شوند پس از مصرف اکسیژن محدود و معین داخل ظرف و آزاد ساختن گازکربنیک دیگر قادر به تنفس عادی نبوده، شروع به تخمیر باقی مانده مواد میکنند. آغاز تخمیر ایجاد اکسیدکربن همراه با اتانول است و بوی اتانول در این هنگام وقوع عمل تخمیر را در محیط کشت معلوم میکند.
C۶H۱۲O۶————>۲C۲H۵OH + ۲CO۲: ∆G = -۳۳ Kcal : تخمیر
C۶H۱۲O۶ + ۶O۲————>۶CO۲ + ۶H۲O: ∆G = ۶۸۶ Kcal : تنفس
تخمیر همیشه با تشکیل الکل همراه نیست، در تخمیر ترکیبات دیگری مانند گلیسیرول نیز بوجود میآیند. پیدایش ترکیبات فرعی غیر از الکل در پدیده تخمیر و حضور این ترکیبات در محیط عمل از نظر ادامه تغییر اهمیت فراوان دارد. رشد مخمرها در شرایط تخمیری (تنفس بیهوازی) بسیار کند است، در شرایط تخمیر انرژی آزاد شده از مقدار معینی مواد قندی مانند یک گرم گلوکز محلول، درحدود ۲۱ بار کمتر از حالت تنفس عادی (هوازی است) انرژی حاصل از پدیده تخمیر بیشتر به صورت حرارت تلف میشود.
محیط در حال تخمیر نسبت به محیطی که در آن تنفس عادی صورت میگیرد بسیار گرمتر است. تخمیر الکلی تحت اثر مجموعه در همی از آنزیمهای درون سلولی به نام (زیماز) صورت میگیرد. مجموعه آنزیمی هنگامی که مخمرهای آن زنده باشند بیشترین اثر تخمیری را دارند. بازده تخمیری آنزیمها در خارج از سلول بسیار ضعیفتر از آنزیمهای داخل سلول زنده است. بین اثر طبیعی آنزیمها، نیروی زیستی و ساختار سلولی مخمرها بستگیهایی وجود دارد و به اصطلاح تخمیر پدیدهای درون سلولی است و آنزیمهای استخراج شده از مخمرها در خارج از سلول بخش مهمی از قدرت تخمیری خود را از دست میدهند.
تخمیر واقعی یا حقیقی
هنگامی در ذخایر قندی یک بافت پیش میآید که در شرایط عادی از هوا قرار داشته، در آن تنفس بی هوازی پیش آید. اگر بخشی از یک بافت ذخیرهای دارای مواد قندی، مانند قطعاتی از غده چغندر بخش از میان بر میوههای آبدار و شیرین مثل انگور را داخل یک ظرف در بسته با مانومتر قرار دهیم، در بافتهای قطعات مزبور ابتدا تنفس عادی با جذب اکسیژن و دفع دیاکسیدکربن صورت میگیرد. از آنجا که اکسیدکربن حاصل از تنفس عادی بعدا در داخل شیره واکوئلی سلولهای بافت حل میشود، فشار داخلی ظرف با جذب اکسیژن موجود به تدریج کم میشود وقتی اکسیژن درون ظرف تمام شده به ناچار شرایط بیهوازی (تخمیر) پیش آمده، با ازدیاد تدریجی اکسیدکربن و الکل در ظرف، بالا رفتن فشار داخلی آن شروع میشود.
تخمیر بهوسیله خود بافتها و بدون حضور میکروارگانیسمها و مخمرها صورت گرفت. این تخمیر که در کلیه بافتهای گیاهی، میوههای سبز مانده در تاریکی و حتی در جلبکها و قارچها نیز کم و بیش دیده میشود تخمیر درون بافتی و عاری از مخمر میگویند. تخمیر درون بافتی در بسیاری از دانههای جوان مانند نخود که پوسته آن نسبت به اکسیژن تا اندازهای قابل نفوذ است و همچنین در بیشتر میوههای آبدار که اکسیژن در بافتهای داخلی آنها معمولاً کم است امری عمومی است.
بویژه اگر مقدار زیادی میوه در یک جا انبار شود، موجبات و شرایط تخمیر در آنها کاملاً فراهم میشود. با توجه به مطالب فوق و تخمیر درون بافتی، باید آن را پدیدهای عمومی در گیاهان دانست و توجه به این امر که آنزیمهای تشکیل دهنده زیماز منشا گیاهی دارند، تخمیر را باید امری طبیعی در گیاهان به شمار آورد. پدیده تخمر درونبافتی با مرگ یاختههای بافت مورد تخمیر معمولاً ارتباط ندارد، اگر بافتهای در حال تخمیر در هوای آزاد قرار داده شوند، تخمیر درونی آنها متوقف شده تنفس عادی مجدداً آغاز میشود. تخمیر در گیاهان فقط از نوع الکلی نیست همراه با ایجاد الکل ترکیبات دیگری مانند جوهر لیمو (اسید سیتریک)، اسید مالیک، اسید اکسالیک و اسید تارتاریک نیز کم و بیش بوجود میآیند.
شدت تخمیر و اندازه گیری آن
شدت تخمیر را با قرار دادن اندام دارای ذخیره قندی مانند دانهها، غدهها و یا میوهها در یک محیط فاقد اکسیژن و دارای ازت میتوان به دقت اندازه گرفت و برای این سنجش از روش اندازه گیری دیاکسیدکربن آزاد شده نیز میتوان استفاده کرد. ولی چون واکنشهای دیگر همزمان با تخمیر میتوانند CO۲ متصاعد کنند این روش ممکن است دقیق نباشد. بنابراین اندازه گیری مقدار الکل تولید شده از تخمیر معمولاً بهتر میتواند معرف و تعیین کننده شدت تخمیر باشد. مقدار الکل حاصل از تخمیر در واحد زمان در یک ترکیب قندی تقریباً معادل همان نسبتی است که از اندازه گیری شدت تنفس به دست میآید.
ساز و کار تخمیر
سازوکار تخمیر الکلی تقریباً مشابه سازوکار (مکانیسم) تنفس عادی است و در بیشتر پیامدهای واکنشی، همانند هم هستند. برای مطالعه مکانیسم تخمیر، به واکنشهای تخمیر الکلی میپردازیم. تخمیر الکلی فقط روی گلوسیدها صورت گرفته، خود شامل دو مرحله است:
مرحله اول انتهای پیامدهای واکنشی که حالت زنجیرهای دارند، همان مسیر EMP یا گلیکولیز است که به تشکیل اسید پیروویک ختم میشود.
مرحله دوم با تجزیه اسید پیروویک که خود سرآغاز پیامدهای واکنشی جداگانهای است که به هیچ وجه ادامه یا بخشی از مسیر گلیکولیز نیست شروع میشود. اسید پیروویک با آنکه در آخر مسیر گلیکولیز و پایان تمام پیامدهای زنجیرهای آن مانند هگزوزها، تری اوزها و همه اوزهای شکسته و تخریب یافته قرار دارد خود از گلوسیدها به شمار نمیآید. شروع تخمیر الکلی از راه گلیکولیز با استالوئید است. استالوئید را میتوان بهوسیله سولفیت سدیم از عصارههای تخمیری به صورت بیسولفیت جدا و استخراج نمود. در تخمیر الکلی به ازای مصرف هر مول گلوکز دو مول NADPH۲ دو مول ATP و دو مول اسید پیروویک حاصل میشود.
در دومین مرحله تخمیر که تبدیل اسیدپیروویک به الکل اتیلیک است NADPH۲ حاصل از مسیر گلیکولیز مصرف و تبدیل شده، از تمام واکنشها فقط دومول ATP که حاصل از فسفریلاسیونهای وابسته به متابولیتهای این مرحله است باقی خواهد ماند واکنش کلی تبدیل گلوکز به الکل اتیلیک بطور خلاصه عبارت است از:
C۶H۱۲O۶ ————>۲CH۳CH۲OH+۲CO۲ + ۲ATP
بازده نظری تخمیر در حدود ۴۴% و کمی بیش از بازده تنفس است. تجزیه گلوکز در واکنشهای تخمیری ناقص بوده از آن فقط ۲ مول ATP حاصل میشود. در فرآیندهای تنفس تجزیه گلوکز بطور کامل صورت گرفته، ۳۶ مول ATP از آن نتیجه میشود.
منبع : دانشنامه رشد
تخمیر
تخمیر پدیدهای است ناشی از مجموعه فعالیتهای زیستی که در آن ترکیبات آلی دارای مولکولهای بزرگ به ترکیبات دارای مولکولهای کوچکتر و سادهتر شکسته و تجزیه (کاتابولیسم) شده از فرآیند آن علاوه بر ایجاد ترکیبات آلی سادهتر، دیاکسیدکربن و انرژی نیز آزاد میگردد. با بیان دیگر تخمیر تجزیه ناقص بعضی از متابولیتها (ترکیبات آلی) به ترکیبات سادهتر همراه با انرژی توسط عامل تخمیری است.
نگاه کلی
در گیاهان تخمیر بیولوژیکی تنها تخمیر الکلی نبوده، ممکن است با کمی تخمیر لاکتیک نیز همراه باشد، برخی از سازوارههای حیاتی (میکروارگانیسمها) مانند قارچهای میکروسکوپی نیز قادر به تخمیرهایی مانند تخمیرهای سیتریک و اکسالیک روی قندهای شش کربنی (هگزوزها) و تخمیر استیک روی الکل اتیلیک و غیره هستند. باکتریها عامل انواع دیگری از تخمیر در طبیعت هستند. تخمیر بوتیریک سلولز لاشه برگها و تجزیه آنها که سبب افزایش ترکیبات آلی خاک میشود و همچنین تخمیرهای تعفنی مواد آلی توسط باکتریها صورت میگیرد.
تخمیر الکلی
پاستور اولین کسی است که نقش مخمرهای الکلی را نشان داد. بهترین مثال مخمرها، مخمرهای خمیرترش یا مخمر نانوایی است. اگر این مخمرها در محیط کشت گلوکز و در حضور اکسیژن کافی قرار گیرند، به شدت تقسیم شده، اکسیژن جذب کرده، دیاکسیدکربن آزاد میسازند. بیشترین سرعت واکنشهای ناشی از تنفس و شدت اکسیداسیون گلوکز این مخمرها که از گروه آسکومیست هستند هنگامی است که تنفس هوازی دارند اگر این مخمرها در داخل یک ظرف در بسته کشت داده شوند پس از مصرف اکسیژن محدود و معین داخل ظرف و آزاد ساختن گازکربنیک دیگر قادر به تنفس عادی نبوده، شروع به تخمیر باقی مانده مواد میکنند. آغاز تخمیر ایجاد اکسیدکربن همراه با اتانول است و بوی اتانول در این هنگام وقوع عمل تخمیر را در محیط کشت معلوم میکند.
C۶H۱۲O۶————>۲C۲H۵OH + ۲CO۲: ∆G = -۳۳ Kcal : تخمیر
C۶H۱۲O۶ + ۶O۲————>۶CO۲ + ۶H۲O: ∆G = ۶۸۶ Kcal : تنفس
تخمیر همیشه با تشکیل الکل همراه نیست، در تخمیر ترکیبات دیگری مانند گلیسیرول نیز بوجود میآیند. پیدایش ترکیبات فرعی غیر از الکل در پدیده تخمیر و حضور این ترکیبات در محیط عمل از نظر ادامه تغییر اهمیت فراوان دارد. رشد مخمرها در شرایط تخمیری (تنفس بیهوازی) بسیار کند است، در شرایط تخمیر انرژی آزاد شده از مقدار معینی مواد قندی مانند یک گرم گلوکز محلول، درحدود ۲۱ بار کمتر از حالت تنفس عادی (هوازی است) انرژی حاصل از پدیده تخمیر بیشتر به صورت حرارت تلف میشود.
محیط در حال تخمیر نسبت به محیطی که در آن تنفس عادی صورت میگیرد بسیار گرمتر است. تخمیر الکلی تحت اثر مجموعه در همی از آنزیمهای درون سلولی به نام (زیماز) صورت میگیرد. مجموعه آنزیمی هنگامی که مخمرهای آن زنده باشند بیشترین اثر تخمیری را دارند. بازده تخمیری آنزیمها در خارج از سلول بسیار ضعیفتر از آنزیمهای داخل سلول زنده است. بین اثر طبیعی آنزیمها، نیروی زیستی و ساختار سلولی مخمرها بستگیهایی وجود دارد و به اصطلاح تخمیر پدیدهای درون سلولی است و آنزیمهای استخراج شده از مخمرها در خارج از سلول بخش مهمی از قدرت تخمیری خود را از دست میدهند.
تخمیر واقعی یا حقیقی
هنگامی در ذخایر قندی یک بافت پیش میآید که در شرایط عادی از هوا قرار داشته، در آن تنفس بی هوازی پیش آید. اگر بخشی از یک بافت ذخیرهای دارای مواد قندی، مانند قطعاتی از غده چغندر بخش از میان بر میوههای آبدار و شیرین مثل انگور را داخل یک ظرف در بسته با مانومتر قرار دهیم، در بافتهای قطعات مزبور ابتدا تنفس عادی با جذب اکسیژن و دفع دیاکسیدکربن صورت میگیرد. از آنجا که اکسیدکربن حاصل از تنفس عادی بعدا در داخل شیره واکوئلی سلولهای بافت حل میشود، فشار داخلی ظرف با جذب اکسیژن موجود به تدریج کم میشود وقتی اکسیژن درون ظرف تمام شده به ناچار شرایط بیهوازی (تخمیر) پیش آمده، با ازدیاد تدریجی اکسیدکربن و الکل در ظرف، بالا رفتن فشار داخلی آن شروع میشود.
تخمیر بهوسیله خود بافتها و بدون حضور میکروارگانیسمها و مخمرها صورت گرفت. این تخمیر که در کلیه بافتهای گیاهی، میوههای سبز مانده در تاریکی و حتی در جلبکها و قارچها نیز کم و بیش دیده میشود تخمیر درون بافتی و عاری از مخمر میگویند. تخمیر درون بافتی در بسیاری از دانههای جوان مانند نخود که پوسته آن نسبت به اکسیژن تا اندازهای قابل نفوذ است و همچنین در بیشتر میوههای آبدار که اکسیژن در بافتهای داخلی آنها معمولاً کم است امری عمومی است.
بویژه اگر مقدار زیادی میوه در یک جا انبار شود، موجبات و شرایط تخمیر در آنها کاملاً فراهم میشود. با توجه به مطالب فوق و تخمیر درون بافتی، باید آن را پدیدهای عمومی در گیاهان دانست و توجه به این امر که آنزیمهای تشکیل دهنده زیماز منشا گیاهی دارند، تخمیر را باید امری طبیعی در گیاهان به شمار آورد. پدیده تخمر درونبافتی با مرگ یاختههای بافت مورد تخمیر معمولاً ارتباط ندارد، اگر بافتهای در حال تخمیر در هوای آزاد قرار داده شوند، تخمیر درونی آنها متوقف شده تنفس عادی مجدداً آغاز میشود. تخمیر در گیاهان فقط از نوع الکلی نیست همراه با ایجاد الکل ترکیبات دیگری مانند جوهر لیمو (اسید سیتریک)، اسید مالیک، اسید اکسالیک و اسید تارتاریک نیز کم و بیش بوجود میآیند.
شدت تخمیر و اندازه گیری آن
شدت تخمیر را با قرار دادن اندام دارای ذخیره قندی مانند دانهها، غدهها و یا میوهها در یک محیط فاقد اکسیژن و دارای ازت میتوان به دقت اندازه گرفت و برای این سنجش از روش اندازه گیری دیاکسیدکربن آزاد شده نیز میتوان استفاده کرد. ولی چون واکنشهای دیگر همزمان با تخمیر میتوانند CO۲ متصاعد کنند این روش ممکن است دقیق نباشد. بنابراین اندازه گیری مقدار الکل تولید شده از تخمیر معمولاً بهتر میتواند معرف و تعیین کننده شدت تخمیر باشد. مقدار الکل حاصل از تخمیر در واحد زمان در یک ترکیب قندی تقریباً معادل همان نسبتی است که از اندازه گیری شدت تنفس به دست میآید.
ساز و کار تخمیر
سازوکار تخمیر الکلی تقریباً مشابه سازوکار (مکانیسم) تنفس عادی است و در بیشتر پیامدهای واکنشی، همانند هم هستند. برای مطالعه مکانیسم تخمیر، به واکنشهای تخمیر الکلی میپردازیم. تخمیر الکلی فقط روی گلوسیدها صورت گرفته، خود شامل دو مرحله است:
مرحله اول انتهای پیامدهای واکنشی که حالت زنجیرهای دارند، همان مسیر EMP یا گلیکولیز است که به تشکیل اسید پیروویک ختم میشود.
مرحله دوم با تجزیه اسید پیروویک که خود سرآغاز پیامدهای واکنشی جداگانهای است که به هیچ وجه ادامه یا بخشی از مسیر گلیکولیز نیست شروع میشود. اسید پیروویک با آنکه در آخر مسیر گلیکولیز و پایان تمام پیامدهای زنجیرهای آن مانند هگزوزها، تری اوزها و همه اوزهای شکسته و تخریب یافته قرار دارد خود از گلوسیدها به شمار نمیآید. شروع تخمیر الکلی از راه گلیکولیز با استالوئید است. استالوئید را میتوان بهوسیله سولفیت سدیم از عصارههای تخمیری به صورت بیسولفیت جدا و استخراج نمود. در تخمیر الکلی به ازای مصرف هر مول گلوکز دو مول NADPH۲ دو مول ATP و دو مول اسید پیروویک حاصل میشود.
در دومین مرحله تخمیر که تبدیل اسیدپیروویک به الکل اتیلیک است NADPH۲ حاصل از مسیر گلیکولیز مصرف و تبدیل شده، از تمام واکنشها فقط دومول ATP که حاصل از فسفریلاسیونهای وابسته به متابولیتهای این مرحله است باقی خواهد ماند واکنش کلی تبدیل گلوکز به الکل اتیلیک بطور خلاصه عبارت است از:
C۶H۱۲O۶ ————>۲CH۳CH۲OH+۲CO۲ + ۲ATP
بازده نظری تخمیر در حدود ۴۴% و کمی بیش از بازده تنفس است. تجزیه گلوکز در واکنشهای تخمیری ناقص بوده از آن فقط ۲ مول ATP حاصل میشود. در فرآیندهای تنفس تجزیه گلوکز بطور کامل صورت گرفته، ۳۶ مول ATP از آن نتیجه میشود.
منبع : دانشنامه رشد
سنتز استیل سالیسیلیک اسید (آسپیرین)
سنتز استیل سالیسیلیک اسید (آسپیرین)
سنتز استیل سالیسیلیک اسید (آسپرین)
بوسیله استیله کردن عامل OH در سالیسیلیک اسید براحتی میتوان آسپرین تهیه کرد. این کار به روشهای متفاوتی امکان پذیر است. یکی از این روشها استفاده از استیک انیدرید در محیط اسیدی میباشد که با توجه به نقش کاتالیستی اسید معمولا در حضور استیک اسید یا سولفوریک اسید انجام میشود.
روش مورد بحث دیگر استفاده از استیل کلرید در حضور پیریدین میباشد.
بخش عملی
الف) سنتز آسپرین با استفاده از استیک انیدرید:
در یک ارلن ۲۵۰ میلی لیتری ۶ گرم سالیسیلیک اسید را با ۹ میلی لیتر استیک انیدرید مخلوط کنید و ۴-۳ قطره سولفوریک اسید غلیظ به آن اضافه کنید. مخلوط واکنش را ضمن هم زدن در یک حمام آب به مدت ۱۵ دقیقه در دمای ۶۰ درجه سانتیگراد حرارت دهید. آن را سرد کرده و در یک بشر حاوی ۱۰۰ میلی لیتر آب سرد همراه با هم زدن بریزید. رسوب را با کمک قیف بوخنر صاف کرده و با آب سرد بشویید. پس از خشک کردن راندمان و نقطه ذوب را تعیین کنید.
برای خالص سازی کامل میتوان بر روی محصول در حلال بنزن تبلور مجدد انجام داد. برای این کار، آب حلال مناسبی نمیباشد. پس از تبلور مجدد راندمان و نقطه ذوب را محاسبه نموده و با مرحله قبل مقایسه کنید.
ب) سنتز آسپرین با استفاده از استیل کلراید:
در یک ارلن ۲۵۰ میلی لیتری ۶ گرم سالیسیلیک اسید را در ۵ میلی لیتر پیریدین حل کنید. ارلن را در حمام یخ بگذارید و ۵ میلی لیتر استیل کلرید را از داخل یک قیف جدا کننده قطره قطره و همراه با بهم زدن شدید به محلول داخل ارلن اضافه کنید. پس از اتمام افزایش، مخلوط واکنش را در یک حمام آب به مدت ۵ دقیقه گرم کنید و سپس سرد نمائید. هنگام سرد کردن یک جسم نیمه جامدی تشکیل میگردد که حدود ۶۰ میلی لیتر آب سرد و چند تکه یخ به آن اضافه کنید و مخلوط را به هم بزنید. کریستالها را با قیف بوخنر صاف کرده و با آب سرد بشویید و سپس خشک کنید. نقطه ذوب و راندمان را محاسبه کرده و بروش قبلی خالص کنید.
آزمایش نیتراسیون سلولز
آزمایش نیتراسیون سلولز
هدف آزمایش
تهیه نیتروسلولز
مثل سایر ترکیبات اورگانیک ، بیشترین منبع سلولز ، بافتهای زنده میباشد. این ترکیب ، در گیاهان ، جانوران و میکروارگانیسمها تولید میشود. پلیمرهای سلولز ، ممکن است از تکرار ۵۰ هزار یا بیشتر از واحدهای ایندروگلوکز ساخته شوند. مهمترین منابع سلولز عبارتند از چوب و کتان. چوب برای ایجاد مواد ساختمانی ، میلیونها تن ، کاغذ و الیاف و مواد شیمیایی بکار میرود. کتان بطور وسیعی از قرن ۱۸ میلادی بعنوان الیاف صنعتی کاربرد دارد.
طبیعت ماکرومولکولی سلولز در ۱۹۲۰ بوسیله Staudinger پیشنهاد شد.
در اثر واکنش گروههای هیدروکسیل در دسترس با تعدادی از اسیدها و انیدریدها ، سلولز “استره” میشود. برای تعدادی از کاربردها ، مهم است که در طول واکنش استریشدن ، حداقل دگراداسیون سلولز رخ میدهد. مخلوط استرهای معدنی و آلی میتوانند در تعدادی از حلالها حل شده و در اثر هیدرولیز تعدادی از محصولات مفید را ایجاد نمایند.
نیترات سلولز بوسیله واکنش سلولز با اسید نیتریک در حضور اسید سولفوریک که تهیه میشود. نیترات سلولز محلول آمورف اسیدی بوده با دانسیتیه ۱٫۶۶gr/lit در آب ، اتانول ، اتر و بنزن نامحلول و در متانول ، نیتروبنزن و حلالهای مخلوط از اتانول- اتر حل میشود.
وسایل مورد نیاز
- سلولز
- اسید نیتریک
- اسید سولفوریک
- بالن و سیستم رفلکس
روش آزمایش
در داخل سیستم رفلکس و داخل بالن ، سلولز و اسید نیتریک را وارد کرده و مقدار کمی اسید سولفوریک به آن بیافزایید و حرارت دهید. رفلکس را آنقدر ادامه دهید تا آب محلول خارج شود و محلول آمورف سفیدی حاصل شود که همان نیترات سلولز است. دانسیته محلول حاصل، ۱٫۶۶gr/lit است.
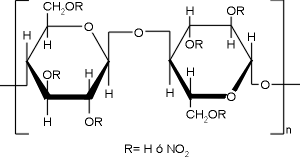
نتیجه
استفاده اصلی نیتروسلولز در تهیه پلاستیکها ، فیلمها و سیمانهاست. نیتروسلولز در صنعت مواد منفجره ، فیبرهای سنتزی (ابریشم چارد و نفت) ، روغنهای هواپیما ، روغن جلای اتومبیل ، شیشه نرم اتومبیل و فیلم عکاسی کاربرد دارد.
آزمایش نیتراسیون سلولز
آزمایش نیتراسیون سلولز
هدف آزمایش
تهیه نیتروسلولز
مثل سایر ترکیبات اورگانیک ، بیشترین منبع سلولز ، بافتهای زنده میباشد. این ترکیب ، در گیاهان ، جانوران و میکروارگانیسمها تولید میشود. پلیمرهای سلولز ، ممکن است از تکرار ۵۰ هزار یا بیشتر از واحدهای ایندروگلوکز ساخته شوند. مهمترین منابع سلولز عبارتند از چوب و کتان. چوب برای ایجاد مواد ساختمانی ، میلیونها تن ، کاغذ و الیاف و مواد شیمیایی بکار میرود. کتان بطور وسیعی از قرن ۱۸ میلادی بعنوان الیاف صنعتی کاربرد دارد.
طبیعت ماکرومولکولی سلولز در ۱۹۲۰ بوسیله Staudinger پیشنهاد شد.
در اثر واکنش گروههای هیدروکسیل در دسترس با تعدادی از اسیدها و انیدریدها ، سلولز “استره” میشود. برای تعدادی از کاربردها ، مهم است که در طول واکنش استریشدن ، حداقل دگراداسیون سلولز رخ میدهد. مخلوط استرهای معدنی و آلی میتوانند در تعدادی از حلالها حل شده و در اثر هیدرولیز تعدادی از محصولات مفید را ایجاد نمایند.
نیترات سلولز بوسیله واکنش سلولز با اسید نیتریک در حضور اسید سولفوریک که تهیه میشود. نیترات سلولز محلول آمورف اسیدی بوده با دانسیتیه ۱٫۶۶gr/lit در آب ، اتانول ، اتر و بنزن نامحلول و در متانول ، نیتروبنزن و حلالهای مخلوط از اتانول- اتر حل میشود.
وسایل مورد نیاز
- سلولز
- اسید نیتریک
- اسید سولفوریک
- بالن و سیستم رفلکس
روش آزمایش
در داخل سیستم رفلکس و داخل بالن ، سلولز و اسید نیتریک را وارد کرده و مقدار کمی اسید سولفوریک به آن بیافزایید و حرارت دهید. رفلکس را آنقدر ادامه دهید تا آب محلول خارج شود و محلول آمورف سفیدی حاصل شود که همان نیترات سلولز است. دانسیته محلول حاصل، ۱٫۶۶gr/lit است.

نتیجه
استفاده اصلی نیتروسلولز در تهیه پلاستیکها ، فیلمها و سیمانهاست. نیتروسلولز در صنعت مواد منفجره ، فیبرهای سنتزی (ابریشم چارد و نفت) ، روغنهای هواپیما ، روغن جلای اتومبیل ، شیشه نرم اتومبیل و فیلم عکاسی کاربرد دارد.
معرفی گروههای عاملی و روشهای شناسایی
معرفی گروههای عاملی و روشهای شناسایی
مقدمه
پیوند کربن-کربن دارای ویژگی غیرعادی مخصوص به خود است.اگر چه اتم های دیگر نیزمی توانند این ویژگی را داشته باشند ولی کاربرد پیوند کربن-کربن بسیار وسیع است .به دلیل این خاصیت منحصربه فرد بیشتر از سه میلیون ترکیبات مختلف حاوی کربن به نام ترکیبات آلی در کتب شیمی گزارش شده اند.در نتیجه جمع آوری دانشی کامل از خواص همه این ترکیبات عملا بسیار سخت است.پیچیدگی ترکیبات آلی را می توان تا حدودی از طریق جمع آوری اطلاعات به دست آمده از گروه های طبیعی این ترکیبات با خواص شیمیایی مشابه تقلیل داد.
این گروه بندی ها توسط اتم یا گروهی از اتم ها که قسمتی از مولکول آلی را تشکیل می دهند شناسایی می شوند.عموما این اتم یا گره اتم را گروه عامل می نامند.پس می توان گروه عاملی را به صورت کامل تری تعریف کرد:
به هر یک از ویژگی های ساختاری که مشخص کننده یک طبقه خاص از ترکیبات آلی باشند گروه عاملی می گویند.
هر گروه عامل نسبت به بقیه مولکول های آلی دارای خواص شیمیایی جداگانه یافت می شوند.
هیدروکربن ها:
ساده ترین گروه در شیمی آلی هیدروکربن ها بوده که ترکیباتی حاوی ات های کربن و هیدروژن می باشند.با توجه به خواص شیمیایی آنها به سه زیرگروه تقسیم می شوند:هیدروکربن های اشباع شده-هیدروکربن های اشباع نشده وهیدروکربن های آروماتیکی.
هیدروکربن های اشباع شده را هم چنین را هم چنین آلکان می نامنددر آلکان ها همه پیوند های کربن-کربن از نوع پیوند ساده بوده که انرژی پیوندی آن در حدود ۳۵۰کیلوژول می باشد.انرژی پیوند های هیدروژن-کربن در حدود ۴۲۰کیلوژول است.پس آلکانها از نظر شیمیایی تقریبا بی اثر می باشد.مهم ترین واکنش آنها سوختن است که آب و دی اکسیدکربن(محصولات سوختن آلکان) تولید می شوند.
هیدروکربن های اشباع نشده دارای ۲زیر گروه آلکنها و آلکینها می باشند.آلکنها دارای یک یا چند پیوند کربن-کربن بوده و آلکینها نیز حاوی یک یا چند پیوند سه گانه کربن-کربن می باشند .پیوند های دو گانه وسه گانه که پیوند های غیر اشباع نامیده می شوند از نظر شیمیایی کاملا واکنش پذیر می باشند.
الکل ها :
یک الکل هیدروکربنی است که در آن یک گروه عامل-OHجانشین یک اتم هیدروژن شده باشد.همچنین یک الکل مانند آبی است که در آن یک گروه آلکیل جانشین یک اتم هیدروژن در یک مولکول آب شده باشند.پس الکل ها خواصی بین خواص اب وهیدروکربن ها دارند.
ساختار الکلها :
فرمول عمومی الکلها ، ROH است که در آن ، R یک گروه آلکیل یا آلکیل استخلاف شده است. این گروه میتواند نوع اول ، دوم یا سوم باشد، ممکن است زنجیرباز یا حلقهای باشد، ممکن است دارای یک اتم هالوژن ، هیدروکسیلهای بیشتر یا یکی از بسیاری گروههای دیگری باشد که فعلا برای ما ناآشنا است.
همه الکلها ، دارای گروه هیدروکسیل (-OH) هستند که بعنوان گروه عاملی ، خواص مشخصه این خانواده از ترکیبها را تعیین میکند. تغییر و تنوع در ساختار R میتواند بر سرعت واکنشهای الکلها و حتی در موارد معدودی بر نوع واکنشها نیز تاثیر گذارد.
خواص فیزیکی الکلها :
دمای جوش در میان هیدروکربنها ، به نظر میرسد که عوامل تعیین کننده دمای جوش ، عمدتا وزن مولکولی و شکل مولکول باشند. در الکلها ، با افزایش تعداد کربن ، دمای جوش بالا میرود و با شاخهدار کردن زنجیر ، دمای جوش پایین میآید، اما نکته غیر عادی در مورد الکلها این است که آنها در دمای بالا به جوش میآیند. این دمای جوش بسیار بالاتر از دمای جوش هیدروکربنها با وزن مولکولی یکسان است و حتی از دمای جوش بسیاری ترکیبها با قطعیت قابل ملاحظه بالاتر است.
دمای جوش بالای آنها ، به علت نیاز به انرژی بیشتر برای شکستن پیوندهای هیدروژنی است که مولکولها را در کنار هم نگه داشتهاند. حل شدن الکلها رفتار الکلها بعنوان حل شده نیز توانایی آنها برای تشکیل پیوندهای هیدروژنی را منعکس میکند. برخلاف هیدروکربنها ، الکلهای سبک با آب امتزاجپذیرند. از آنجا که نیروهای بین مولکولی الکلها همانند نیروهای بین مولکولی آب است، دو نوع مولکول با یکدیگر قابل اختلاط هستند. انرژی لازم برای شکستن یک پیوند هیدروژنی بین دو مولکول آب یا دو مولکول الکل ، با تشکیل یک پیوند هیدروژنی بین یک مولکول آب و یک مولکول الکل تامین میشود.
آلدهید:
یک آلدهید دارای گروه عامل –CHOدر مولکول آلی می باشد.کلمه آلدهید(Aldehyde)از دو اژه الکل وهیدروژن گیری گرفته شده است.هرگاه از الکل نوع اول هیدروژن گیری شود در آن صورت تولید می گردد که آلدهید نامیده می شود.
کتون:(ketone)
یک کتون یک گروه عاملی است که با یک گروه کربونیل که با دو اتم کربن دیگر پیوند دارد ؛ شناخته میشود. یک کتون را میتوان با فرمول R۱(CO)R۲ بیان کرد. اتم کربن که با دو اتم کربن پیوند دارد آن را از گروههای عاملی کربوکسیلیک اسیدها ، آلدهیدها، استرها، آمیدها و دیگر ترکیبهای اکسیژندار جدا میکند. پیوند دوگانهٔ گروه کربونیل نیز کتونها را از الکل ها و اترها باز میشناساند.
به کربنی که به کربن گروه کربونیل چسبیده کربن آلفا و به هیدروژنی که به این کربن چسبیده هیدروژن آلفا گویند. در حضور یک کاتالیزور اسیدی کتون به keto-enol tautomerism مربوط میشود. واکنش با یک پایه قوی انول متناظر را نتیجه میدهد.
خواص شیمیایی آلدهید ها و کتون ها:
آلدهید ها وکتون ها در چند نوع فعل و انفعال شرکت می کنند که اهم آن به قرار زیر است:
۱)حمله الکترونخواهی اسیدهای لوئیس روی اکسیژن گروه کربونیل موجب افزایش دانسیته بار مثبت کربن گروه کربونیل می شود که در نهایت موجب افزایش خصلت اسیدی پروتون ههای کربن های آلفای کربونیل می گردد.صحت این نکته به وسیله روش های افزاری تائید شده است.
۲)حمله هسته خواهی برکربن گروه کربونیل دومین دسته وسیع از واکنشهای آلدهید ها وکتون ها را تشکیل می دهد.به عنوان مثال از افزایش آب بر آلدهید ها وکتون ها دیول دوقلو(gemdiol)ایجاد می شود و درصد تشکیل آن به ساختمان ماده و به پایداری محصول حاصل بستگی دارد.به عنوان مثال مقدار دیول دوقلوی حاصل از استون در دمای ۲۰درجه سانتی گراد خیلی کم و قابل اغماض است در صورتیکه آلدهید فرمیک و تری کلرو استالدهید به خوبی و به طور کامل به دیول دو قلو تبدیل می شوند.
تهیه آلدهید ها و کتون ها از راه اکسایش الکل ها:
مصرف زیاد آلدهید و کتون در سنتزهای آلی باعث می شود که نحوه تهیه آنها اهمیت بسیاری داشته باشد.این اجسام را می توان از آلکین ها –کربوکسیلیک اسیدها و مشتق کربوکسیلیک اسیدها سنتز کرد.آلکینها دراثرآبدارکردن باکاتالیزور اسید به وسیله هیدروبوردارکردن-اکسایش به آلدهید یا کتون تبدیل می شوند.
کربوکسیلیک اسیدها یا مشتقات آنها با ترکیبات آلی فلزدار یا معرف های کاهند دیگر ترکیب می شوند و آلدهید یا کتون می دهند.با وجود این یکی از معمولترین روش های سنتزی اکسایش الکل های نوع اول و دوم با کرومیک اسید H2CrO4 یا پتاسیم پرمنگنات است.
در این گزارش کار نحوه مصرف کرومیک اسید در تبدیل الکلها به آلدهید ها و کتون ها مورد بحث قرار می گیرد.
کرومیک اسید برای مدت طولانی پایدار نیست و بنابراین آن را در هنگام لزوم از ترکیب سدیم یا پتاسیم دی کرومات با اسید اضافی مانند سولفوریک یا اسد استیک یا با انحلال کرومیک انیدرید در آب تهیه می کنند.
در روش اخیر سولفوریک اسید یا استیک اسید نیز اضافه می شود زیرا که سرعت اکسایش الکل ها با کرومیک اسید در محلول اسیدی بسیار زیادتر است.در تهیه یا اکسایش اجسامی که در محیط اسیدی قوی تجزیه می شوند کرومیک انیدریدرا در پیریدین حل می کنند یا پتاسیم پرمنگنات بازی را به عنوان معرف اکسید کننده به کار می برند.
الکلها در مجاورت کرومیک اسید به استر تبدیل می شوند.این عمل کاملا به واکنش الکل ها وکربوکسیلیک اسیدها شباهت دارد.
وجود چند واکنش جانبی مهم اکسایش الکل نوع اول به آلدهید را پیچیده می کند.
به احتمال زیاد مهمترین واکنش جانبی اکسایش سریع آلدهید با کرومیک اسید و تبدیل آن به کربوکسیلیک اسید است.برای تقلیل این اکسایش اضافی نامطلوب کرومیک اسید را به الکل نوع اول اضافه می کنند تا عامل اکسنده اضافی در مخلوط واکنش موجود نباشد وهم چنین آلدهیدرا در هنگام تشکیل از مخلوط واکنش تقطیر می کنند.بنابراین چنان چه در اکسایش با کرو میک اسید لازم باشد که آلدهید با بازده زیادی تهیه می شودباید آلدهید موردنظر خیلی فرارباشد یعنی در کمتر از حدود ۱۵۰بجوشد.
کتون ها در محیط اسیدی ملایم در برابر این اکسنده بسیار پایدارتر از آلدهیدها هستند از این رو در تبدیل الکل های نوع دوم به کتون ها میزان واکنش های جانبی که در اکسایش الکل های نوع اول گفته شد چندان قابل ملاحظه نیستند.ولی در شرایط بازی یا اسیدی قوی کتون هایی که به فرم انولی در می آیند اکسید می شوند و به دو قسمت کربونیل دار تجزیه می شوند.برای مثال می توان سیکلو هگزانول را با کرومیک اسید اکسیدکرد وبازده زیادی از سیکلوهگزانون به دست آورد ولی این جسم در اثر ترکیب با پتاسیم پرمنگنات در محیط بازی ضعیف به آدیپیک اسید تبدیل می شود.بدون شک در این واکنش ابتدا کتون به یون انولات تبدیل می شود تبدیل می شودو بعداین یون با پرمنگنات اکسید می شود.
سیکلوهگزانون یک کتون متقارن است و فقط یک یون انولات می دهد.چنان چه کتون متقارن نباشد دو یون انولات متفاوت تولی می شود وهر یک از آنها با پرمنگنات به محصول جداگانه ای اکسید می شود.در اکسایش کتون های نامتقارن مخلوط پیچیده ای از چند محصول تشکیل می شود وچنین مشکلی مصرف سنتزی این واکنش ها را کم می کند.
استرها:
یک استر از واکنش یک اسید آلی با یک الکل تولید می شود.استرها دارای گروه عامل-COO-بوده که از یک پیوند دوگانه کربن-اکسیژن(-C=O)ویک پیوند ساده کربن-اکسیژن(C-O-)تشکیل شده اند.اغلب استرها فرار هستندودارای بوی مطبوعی می باشند.رایحه طبیعی بسیاری از گلها وطعم بسیاری ازمیوه ها به حضور یک یا چند استر بستگی دارد.بعضی از استرهای طبیعی مهم در چربی وروغن ها(روغم برزک-روغن دانه پنبه-روغن زیتون)در سنتزمارگارین(کره نباتی)کره بادام زمینی وعصاره ی سبزیجات به کار می روند.
شناسایی گروههای عاملی
در شناسایی یک جسم مجهول پس از تجزیه و تعیین خواص فیزیکی آن با توجه به نتایج حاصله باید آزمایشات شناسایی گروههای عاملی را روی نمونه انجام داد. مثلا اگر در تجزیه عنصری نمونه وجود O اثبات شده، حال این مسئله پیش می آید که اکسیژن ممکن است به صورت گروه –C=O یا –OH یا C–O–C و یا غیره باشد. بنابر این یک سری آزمایشات برای تشخیص گروه عاملی نمونه لازم است. نکته ای که معمولا باید به آن توجه کرد این است که چنانچه در انجام آزماشات برای حل کردن نمونه از یک حلال استفاده نمودید برای اطمینان خاطر برای اینکه حتما بدانید که حلال با معرف وارد واکنش نشده یک شاهد تهیه کنید. بدین ترتیب که در یک لوله مقداری حلال ریخته و به همان اندازه معرفی اضافه کنید که به محلول شامل حلال و نمونه مورد نظر اضافه نموده اید و دو لوله را با یکدیگر مقایسه کنید.
بخش عملی:
شناسایی آلکنها:
الف) آزمایش برم در استیک اسید: در یک لوله آزمایش ۱ میلی لیتر سیکلوهگزن ریخته و به آن محلول Br2/CH3COOH قطره قطره اضافه کنید، با از بین رفتن رنگ برم میتوان نتیجه گرفت که برم در واکنش شیمیایی شرکت کرده و مصرف میشود
ب) پرمنگنات پتاسیم: یک قطره سیکلوهگزن را در ۲ میلی لیتر آب حل کرده و به آن ۳ قطره محلول KMnO4 اضافه نمائید و محلول را خوب به هم زده و نتیجه مشاهده شده را یادداشت کنید.
شناسایی الکلها:
الف) حلالیت: ۶ لوله آزمایش برداشته و در هر کدام ۱ میلی لیتر آب ریخته و هر یک از الکلهای زیر ر ا به یکی از لوله ها اضافه کنید و هم بزنید. ۱) متانول ۲) اتانول ۳) پروپانول ۴) نرمال بوتانول ۵) بوتان ۲-اُل ۶) ۲-متیل پروپان ۲ – اُل
سپس این آزمایش را برای حلال هگزان تکرار کنید و نتایج هر کدام را بنویسید.
ب) انیدریدکرومیک: ۳-۱ میلی لیتر از هر یک از الکلهای فوق را در لوله آزمایش ریخته به آن یک الی دو قطره معرف انیدرید کرومیک اضافه کنید. تشکیل رسوب سبز مایل به آبی دلیل بر مثبت بودن آزمایش است. این آزمایش برای الکلهای نوع اول و دوم جواب مثبت میدهد.
ج) یدوفرم: در یک لوله آزمایش ۵/۰ میلی لیتر اتانول ریخته بدان ۱mL سود ۱۰% افزوده و آنقدر به محلول اخیر محلول ید در یدید پتاسیم (I2/KI) اضافه کنید تا رنگ قهوه ای محلول اخیر باقی بماند. بعد رنگ ید اضافی را با یک قطره سود ۱۰% همراه با تکان دادن از بین ببرید. حال لوله را از آب پر کرده و آنرا برای ۱۵ دقیقه به حال خود بگذارید. تشکیل رسوب زرد لیموئی (رسوب یدوفرم) دلیل بر مثبت بودن آزمایش است.
این آزمایش را برای متانول – نرمال بوتانول – استن – بنزآلدئید – استوفنون – ترشری بوتیل الکل انجام دهید.
د) استری شدن الکلها توسط اسیدهای آلی: یک قطره از استیک اسید غلیظ را وارد ۱mL اتانول نموده و قطره ای اسید سولفوریک غلیظ بدان اضافه کنید حال محلول را در حمام آب گرم حرارت داده تا بجوش آید، پس از مدتی بوی مخصوصی به مشام میرسد. نوع بوی حس شده را با بوی اسید مقایسه کنید.
آزمایش لوکاس: بر روی نیم میلی لیتر از ترشری بوتیل الکل ۳ میلی لیتر اسید کلریدریک غلیظ بریزید. محلول ابتدا بیرنگ است ولی کم کم کدر شده و رسوب میدهد. مشخصات رسوب را نوشته و این آزمایش را برای اتانول و بوتان ۲-اُل هم انجام دهید.
شناسایی آلدئیدها و کتونها
الف) ۲، ۴ دی نیترو فنیل هیدرازین: ۱ میلی لیتر استن در لوله آزمایش ریخته و بدان چند قطره معرف ۲، ۴ دی نیتروفنیل هیدرازین اضافه کنید و مشاهده خود را یادداشت کنید. این آزمایش را روی بنزآلدئید و استوفنون نیز انجام دهید. این آزمایش به آلدئیدها و کتونها جواب میدهد.
ب) سدیم بی سولفیت: یک میلی لیتر از معرف غلیظ را در یک لوله آزمایش ریخته به آن ۳/۰ میلی لیتر از جسم مورد نظر اضافه کنید و شدیدا تکان دهید، تشکیل رسوب سفید دلیل بر مثبت بودن آزمایش است. اکثر گروههای کربونیل فعال به این آزمایش جواب مثبت میدهند، چون این واکنش نوکلئوفیلی است هرچقدر گروه کربنیل مثبت تر باشد امکان جواب مثبت بیشتر است، در نتیجه این آزمایش بیشتر مخصوص آلدئیدها میباشد. این آزمایش را برای استون و بنزآلدئید انجام دهید.
ج) تالنز: ۱ میلی لیتر بنزآلدئید در لوله آزمایش ریخته و به آن ۱ میلی لیتر از معرف تازه تهیه شده اضافه کنید. در صورت لزوم کمی حرارت دهید (توسط حمام آب گرم ملایم) تشکیل آئینه نقره ای مثبت بودن آزمایش را نشان میدهد.
د) معرف کرومیک اسید: ۱ قطره از جسم مایع یا یک صدم گرم از جسم جامد را در ۱ میلی لیتر استون حل کنید و چند قطره معرف به آن اضافه نمائید.
معرف اسید کرومیک
۲۵ گرم انیدرید کرومیک CrO3 را در ۲۵ سی سی اسید سولفوریک غلیظ حل کنید و به هم بزنید تا خمیر یکنواختی به دست آید، بعد محلول حاصل را بوسیله ۷۵ سی سی آب مقطر با احتیاط رقیق نمائید. رنگ معرف نارنجی روشن است.
منبع :
کتاب آزمایشگاه شیمی عمومی۲ نویسندگان:جو.ا.برن-جیمزای.بردی – مترجمان:لیلا حجت کاشانی-دکتر رحمت الله رحیمی
کتاب شیمی آلی تجربی نوین – نام نویسندگان:رابرتس-گیلبرت-ردوالد-وینگرو-نام مترجم:هوشنگ پیر الهی
www.en.wikipedia.org/wiki/Ketone
معرفی گروههای عاملی و روشهای شناسایی
معرفی گروههای عاملی و روشهای شناسایی
مقدمه
پیوند کربن-کربن دارای ویژگی غیرعادی مخصوص به خود است.اگر چه اتم های دیگر نیزمی توانند این ویژگی را داشته باشند ولی کاربرد پیوند کربن-کربن بسیار وسیع است .به دلیل این خاصیت منحصربه فرد بیشتر از سه میلیون ترکیبات مختلف حاوی کربن به نام ترکیبات آلی در کتب شیمی گزارش شده اند.در نتیجه جمع آوری دانشی کامل از خواص همه این ترکیبات عملا بسیار سخت است.پیچیدگی ترکیبات آلی را می توان تا حدودی از طریق جمع آوری اطلاعات به دست آمده از گروه های طبیعی این ترکیبات با خواص شیمیایی مشابه تقلیل داد.
این گروه بندی ها توسط اتم یا گروهی از اتم ها که قسمتی از مولکول آلی را تشکیل می دهند شناسایی می شوند.عموما این اتم یا گره اتم را گروه عامل می نامند.پس می توان گروه عاملی را به صورت کامل تری تعریف کرد:
به هر یک از ویژگی های ساختاری که مشخص کننده یک طبقه خاص از ترکیبات آلی باشند گروه عاملی می گویند.
هر گروه عامل نسبت به بقیه مولکول های آلی دارای خواص شیمیایی جداگانه یافت می شوند.
هیدروکربن ها:
ساده ترین گروه در شیمی آلی هیدروکربن ها بوده که ترکیباتی حاوی ات های کربن و هیدروژن می باشند.با توجه به خواص شیمیایی آنها به سه زیرگروه تقسیم می شوند:هیدروکربن های اشباع شده-هیدروکربن های اشباع نشده وهیدروکربن های آروماتیکی.
هیدروکربن های اشباع شده را هم چنین را هم چنین آلکان می نامنددر آلکان ها همه پیوند های کربن-کربن از نوع پیوند ساده بوده که انرژی پیوندی آن در حدود ۳۵۰کیلوژول می باشد.انرژی پیوند های هیدروژن-کربن در حدود ۴۲۰کیلوژول است.پس آلکانها از نظر شیمیایی تقریبا بی اثر می باشد.مهم ترین واکنش آنها سوختن است که آب و دی اکسیدکربن(محصولات سوختن آلکان) تولید می شوند.
هیدروکربن های اشباع نشده دارای ۲زیر گروه آلکنها و آلکینها می باشند.آلکنها دارای یک یا چند پیوند کربن-کربن بوده و آلکینها نیز حاوی یک یا چند پیوند سه گانه کربن-کربن می باشند .پیوند های دو گانه وسه گانه که پیوند های غیر اشباع نامیده می شوند از نظر شیمیایی کاملا واکنش پذیر می باشند.
الکل ها :
یک الکل هیدروکربنی است که در آن یک گروه عامل-OHجانشین یک اتم هیدروژن شده باشد.همچنین یک الکل مانند آبی است که در آن یک گروه آلکیل جانشین یک اتم هیدروژن در یک مولکول آب شده باشند.پس الکل ها خواصی بین خواص اب وهیدروکربن ها دارند.
ساختار الکلها :
فرمول عمومی الکلها ، ROH است که در آن ، R یک گروه آلکیل یا آلکیل استخلاف شده است. این گروه میتواند نوع اول ، دوم یا سوم باشد، ممکن است زنجیرباز یا حلقهای باشد، ممکن است دارای یک اتم هالوژن ، هیدروکسیلهای بیشتر یا یکی از بسیاری گروههای دیگری باشد که فعلا برای ما ناآشنا است.
همه الکلها ، دارای گروه هیدروکسیل (-OH) هستند که بعنوان گروه عاملی ، خواص مشخصه این خانواده از ترکیبها را تعیین میکند. تغییر و تنوع در ساختار R میتواند بر سرعت واکنشهای الکلها و حتی در موارد معدودی بر نوع واکنشها نیز تاثیر گذارد.
خواص فیزیکی الکلها :
دمای جوش در میان هیدروکربنها ، به نظر میرسد که عوامل تعیین کننده دمای جوش ، عمدتا وزن مولکولی و شکل مولکول باشند. در الکلها ، با افزایش تعداد کربن ، دمای جوش بالا میرود و با شاخهدار کردن زنجیر ، دمای جوش پایین میآید، اما نکته غیر عادی در مورد الکلها این است که آنها در دمای بالا به جوش میآیند. این دمای جوش بسیار بالاتر از دمای جوش هیدروکربنها با وزن مولکولی یکسان است و حتی از دمای جوش بسیاری ترکیبها با قطعیت قابل ملاحظه بالاتر است.
دمای جوش بالای آنها ، به علت نیاز به انرژی بیشتر برای شکستن پیوندهای هیدروژنی است که مولکولها را در کنار هم نگه داشتهاند. حل شدن الکلها رفتار الکلها بعنوان حل شده نیز توانایی آنها برای تشکیل پیوندهای هیدروژنی را منعکس میکند. برخلاف هیدروکربنها ، الکلهای سبک با آب امتزاجپذیرند. از آنجا که نیروهای بین مولکولی الکلها همانند نیروهای بین مولکولی آب است، دو نوع مولکول با یکدیگر قابل اختلاط هستند. انرژی لازم برای شکستن یک پیوند هیدروژنی بین دو مولکول آب یا دو مولکول الکل ، با تشکیل یک پیوند هیدروژنی بین یک مولکول آب و یک مولکول الکل تامین میشود.
آلدهید:
یک آلدهید دارای گروه عامل –CHOدر مولکول آلی می باشد.کلمه آلدهید(Aldehyde)از دو اژه الکل وهیدروژن گیری گرفته شده است.هرگاه از الکل نوع اول هیدروژن گیری شود در آن صورت تولید می گردد که آلدهید نامیده می شود.
کتون:(ketone)
یک کتون یک گروه عاملی است که با یک گروه کربونیل که با دو اتم کربن دیگر پیوند دارد ؛ شناخته میشود. یک کتون را میتوان با فرمول R۱(CO)R۲ بیان کرد. اتم کربن که با دو اتم کربن پیوند دارد آن را از گروههای عاملی کربوکسیلیک اسیدها ، آلدهیدها، استرها، آمیدها و دیگر ترکیبهای اکسیژندار جدا میکند. پیوند دوگانهٔ گروه کربونیل نیز کتونها را از الکل ها و اترها باز میشناساند.
به کربنی که به کربن گروه کربونیل چسبیده کربن آلفا و به هیدروژنی که به این کربن چسبیده هیدروژن آلفا گویند. در حضور یک کاتالیزور اسیدی کتون به keto-enol tautomerism مربوط میشود. واکنش با یک پایه قوی انول متناظر را نتیجه میدهد.
خواص شیمیایی آلدهید ها و کتون ها:
آلدهید ها وکتون ها در چند نوع فعل و انفعال شرکت می کنند که اهم آن به قرار زیر است:
۱)حمله الکترونخواهی اسیدهای لوئیس روی اکسیژن گروه کربونیل موجب افزایش دانسیته بار مثبت کربن گروه کربونیل می شود که در نهایت موجب افزایش خصلت اسیدی پروتون ههای کربن های آلفای کربونیل می گردد.صحت این نکته به وسیله روش های افزاری تائید شده است.
۲)حمله هسته خواهی برکربن گروه کربونیل دومین دسته وسیع از واکنشهای آلدهید ها وکتون ها را تشکیل می دهد.به عنوان مثال از افزایش آب بر آلدهید ها وکتون ها دیول دوقلو(gemdiol)ایجاد می شود و درصد تشکیل آن به ساختمان ماده و به پایداری محصول حاصل بستگی دارد.به عنوان مثال مقدار دیول دوقلوی حاصل از استون در دمای ۲۰درجه سانتی گراد خیلی کم و قابل اغماض است در صورتیکه آلدهید فرمیک و تری کلرو استالدهید به خوبی و به طور کامل به دیول دو قلو تبدیل می شوند.
تهیه آلدهید ها و کتون ها از راه اکسایش الکل ها:
مصرف زیاد آلدهید و کتون در سنتزهای آلی باعث می شود که نحوه تهیه آنها اهمیت بسیاری داشته باشد.این اجسام را می توان از آلکین ها –کربوکسیلیک اسیدها و مشتق کربوکسیلیک اسیدها سنتز کرد.آلکینها دراثرآبدارکردن باکاتالیزور اسید به وسیله هیدروبوردارکردن-اکسایش به آلدهید یا کتون تبدیل می شوند.
کربوکسیلیک اسیدها یا مشتقات آنها با ترکیبات آلی فلزدار یا معرف های کاهند دیگر ترکیب می شوند و آلدهید یا کتون می دهند.با وجود این یکی از معمولترین روش های سنتزی اکسایش الکل های نوع اول و دوم با کرومیک اسید H2CrO4 یا پتاسیم پرمنگنات است.
در این گزارش کار نحوه مصرف کرومیک اسید در تبدیل الکلها به آلدهید ها و کتون ها مورد بحث قرار می گیرد.
کرومیک اسید برای مدت طولانی پایدار نیست و بنابراین آن را در هنگام لزوم از ترکیب سدیم یا پتاسیم دی کرومات با اسید اضافی مانند سولفوریک یا اسد استیک یا با انحلال کرومیک انیدرید در آب تهیه می کنند.
در روش اخیر سولفوریک اسید یا استیک اسید نیز اضافه می شود زیرا که سرعت اکسایش الکل ها با کرومیک اسید در محلول اسیدی بسیار زیادتر است.در تهیه یا اکسایش اجسامی که در محیط اسیدی قوی تجزیه می شوند کرومیک انیدریدرا در پیریدین حل می کنند یا پتاسیم پرمنگنات بازی را به عنوان معرف اکسید کننده به کار می برند.
الکلها در مجاورت کرومیک اسید به استر تبدیل می شوند.این عمل کاملا به واکنش الکل ها وکربوکسیلیک اسیدها شباهت دارد.
وجود چند واکنش جانبی مهم اکسایش الکل نوع اول به آلدهید را پیچیده می کند.
به احتمال زیاد مهمترین واکنش جانبی اکسایش سریع آلدهید با کرومیک اسید و تبدیل آن به کربوکسیلیک اسید است.برای تقلیل این اکسایش اضافی نامطلوب کرومیک اسید را به الکل نوع اول اضافه می کنند تا عامل اکسنده اضافی در مخلوط واکنش موجود نباشد وهم چنین آلدهیدرا در هنگام تشکیل از مخلوط واکنش تقطیر می کنند.بنابراین چنان چه در اکسایش با کرو میک اسید لازم باشد که آلدهید با بازده زیادی تهیه می شودباید آلدهید موردنظر خیلی فرارباشد یعنی در کمتر از حدود ۱۵۰بجوشد.
کتون ها در محیط اسیدی ملایم در برابر این اکسنده بسیار پایدارتر از آلدهیدها هستند از این رو در تبدیل الکل های نوع دوم به کتون ها میزان واکنش های جانبی که در اکسایش الکل های نوع اول گفته شد چندان قابل ملاحظه نیستند.ولی در شرایط بازی یا اسیدی قوی کتون هایی که به فرم انولی در می آیند اکسید می شوند و به دو قسمت کربونیل دار تجزیه می شوند.برای مثال می توان سیکلو هگزانول را با کرومیک اسید اکسیدکرد وبازده زیادی از سیکلوهگزانون به دست آورد ولی این جسم در اثر ترکیب با پتاسیم پرمنگنات در محیط بازی ضعیف به آدیپیک اسید تبدیل می شود.بدون شک در این واکنش ابتدا کتون به یون انولات تبدیل می شود تبدیل می شودو بعداین یون با پرمنگنات اکسید می شود.
سیکلوهگزانون یک کتون متقارن است و فقط یک یون انولات می دهد.چنان چه کتون متقارن نباشد دو یون انولات متفاوت تولی می شود وهر یک از آنها با پرمنگنات به محصول جداگانه ای اکسید می شود.در اکسایش کتون های نامتقارن مخلوط پیچیده ای از چند محصول تشکیل می شود وچنین مشکلی مصرف سنتزی این واکنش ها را کم می کند.
استرها:
یک استر از واکنش یک اسید آلی با یک الکل تولید می شود.استرها دارای گروه عامل-COO-بوده که از یک پیوند دوگانه کربن-اکسیژن(-C=O)ویک پیوند ساده کربن-اکسیژن(C-O-)تشکیل شده اند.اغلب استرها فرار هستندودارای بوی مطبوعی می باشند.رایحه طبیعی بسیاری از گلها وطعم بسیاری ازمیوه ها به حضور یک یا چند استر بستگی دارد.بعضی از استرهای طبیعی مهم در چربی وروغن ها(روغم برزک-روغن دانه پنبه-روغن زیتون)در سنتزمارگارین(کره نباتی)کره بادام زمینی وعصاره ی سبزیجات به کار می روند.
شناسایی گروههای عاملی
در شناسایی یک جسم مجهول پس از تجزیه و تعیین خواص فیزیکی آن با توجه به نتایج حاصله باید آزمایشات شناسایی گروههای عاملی را روی نمونه انجام داد. مثلا اگر در تجزیه عنصری نمونه وجود O اثبات شده، حال این مسئله پیش می آید که اکسیژن ممکن است به صورت گروه –C=O یا –OH یا C–O–C و یا غیره باشد. بنابر این یک سری آزمایشات برای تشخیص گروه عاملی نمونه لازم است. نکته ای که معمولا باید به آن توجه کرد این است که چنانچه در انجام آزماشات برای حل کردن نمونه از یک حلال استفاده نمودید برای اطمینان خاطر برای اینکه حتما بدانید که حلال با معرف وارد واکنش نشده یک شاهد تهیه کنید. بدین ترتیب که در یک لوله مقداری حلال ریخته و به همان اندازه معرفی اضافه کنید که به محلول شامل حلال و نمونه مورد نظر اضافه نموده اید و دو لوله را با یکدیگر مقایسه کنید.
بخش عملی:
شناسایی آلکنها:
الف) آزمایش برم در استیک اسید: در یک لوله آزمایش ۱ میلی لیتر سیکلوهگزن ریخته و به آن محلول Br2/CH3COOH قطره قطره اضافه کنید، با از بین رفتن رنگ برم میتوان نتیجه گرفت که برم در واکنش شیمیایی شرکت کرده و مصرف میشود
ب) پرمنگنات پتاسیم: یک قطره سیکلوهگزن را در ۲ میلی لیتر آب حل کرده و به آن ۳ قطره محلول KMnO4 اضافه نمائید و محلول را خوب به هم زده و نتیجه مشاهده شده را یادداشت کنید.
شناسایی الکلها:
الف) حلالیت: ۶ لوله آزمایش برداشته و در هر کدام ۱ میلی لیتر آب ریخته و هر یک از الکلهای زیر ر ا به یکی از لوله ها اضافه کنید و هم بزنید. ۱) متانول ۲) اتانول ۳) پروپانول ۴) نرمال بوتانول ۵) بوتان ۲-اُل ۶) ۲-متیل پروپان ۲ – اُل
سپس این آزمایش را برای حلال هگزان تکرار کنید و نتایج هر کدام را بنویسید.
ب) انیدریدکرومیک: ۳-۱ میلی لیتر از هر یک از الکلهای فوق را در لوله آزمایش ریخته به آن یک الی دو قطره معرف انیدرید کرومیک اضافه کنید. تشکیل رسوب سبز مایل به آبی دلیل بر مثبت بودن آزمایش است. این آزمایش برای الکلهای نوع اول و دوم جواب مثبت میدهد.
ج) یدوفرم: در یک لوله آزمایش ۵/۰ میلی لیتر اتانول ریخته بدان ۱mL سود ۱۰% افزوده و آنقدر به محلول اخیر محلول ید در یدید پتاسیم (I2/KI) اضافه کنید تا رنگ قهوه ای محلول اخیر باقی بماند. بعد رنگ ید اضافی را با یک قطره سود ۱۰% همراه با تکان دادن از بین ببرید. حال لوله را از آب پر کرده و آنرا برای ۱۵ دقیقه به حال خود بگذارید. تشکیل رسوب زرد لیموئی (رسوب یدوفرم) دلیل بر مثبت بودن آزمایش است.
این آزمایش را برای متانول – نرمال بوتانول – استن – بنزآلدئید – استوفنون – ترشری بوتیل الکل انجام دهید.
د) استری شدن الکلها توسط اسیدهای آلی: یک قطره از استیک اسید غلیظ را وارد ۱mL اتانول نموده و قطره ای اسید سولفوریک غلیظ بدان اضافه کنید حال محلول را در حمام آب گرم حرارت داده تا بجوش آید، پس از مدتی بوی مخصوصی به مشام میرسد. نوع بوی حس شده را با بوی اسید مقایسه کنید.
آزمایش لوکاس: بر روی نیم میلی لیتر از ترشری بوتیل الکل ۳ میلی لیتر اسید کلریدریک غلیظ بریزید. محلول ابتدا بیرنگ است ولی کم کم کدر شده و رسوب میدهد. مشخصات رسوب را نوشته و این آزمایش را برای اتانول و بوتان ۲-اُل هم انجام دهید.
شناسایی آلدئیدها و کتونها
الف) ۲، ۴ دی نیترو فنیل هیدرازین: ۱ میلی لیتر استن در لوله آزمایش ریخته و بدان چند قطره معرف ۲، ۴ دی نیتروفنیل هیدرازین اضافه کنید و مشاهده خود را یادداشت کنید. این آزمایش را روی بنزآلدئید و استوفنون نیز انجام دهید. این آزمایش به آلدئیدها و کتونها جواب میدهد.
ب) سدیم بی سولفیت: یک میلی لیتر از معرف غلیظ را در یک لوله آزمایش ریخته به آن ۳/۰ میلی لیتر از جسم مورد نظر اضافه کنید و شدیدا تکان دهید، تشکیل رسوب سفید دلیل بر مثبت بودن آزمایش است. اکثر گروههای کربونیل فعال به این آزمایش جواب مثبت میدهند، چون این واکنش نوکلئوفیلی است هرچقدر گروه کربنیل مثبت تر باشد امکان جواب مثبت بیشتر است، در نتیجه این آزمایش بیشتر مخصوص آلدئیدها میباشد. این آزمایش را برای استون و بنزآلدئید انجام دهید.
ج) تالنز: ۱ میلی لیتر بنزآلدئید در لوله آزمایش ریخته و به آن ۱ میلی لیتر از معرف تازه تهیه شده اضافه کنید. در صورت لزوم کمی حرارت دهید (توسط حمام آب گرم ملایم) تشکیل آئینه نقره ای مثبت بودن آزمایش را نشان میدهد.
د) معرف کرومیک اسید: ۱ قطره از جسم مایع یا یک صدم گرم از جسم جامد را در ۱ میلی لیتر استون حل کنید و چند قطره معرف به آن اضافه نمائید.
معرف اسید کرومیک
۲۵ گرم انیدرید کرومیک CrO3 را در ۲۵ سی سی اسید سولفوریک غلیظ حل کنید و به هم بزنید تا خمیر یکنواختی به دست آید، بعد محلول حاصل را بوسیله ۷۵ سی سی آب مقطر با احتیاط رقیق نمائید. رنگ معرف نارنجی روشن است.
منبع :
کتاب آزمایشگاه شیمی عمومی۲ نویسندگان:جو.ا.برن-جیمزای.بردی – مترجمان:لیلا حجت کاشانی-دکتر رحمت الله رحیمی
کتاب شیمی آلی تجربی نوین – نام نویسندگان:رابرتس-گیلبرت-ردوالد-وینگرو-نام مترجم:هوشنگ پیر الهی
www.en.wikipedia.org/wiki/Ketone
شناسایی هالوژنها در ترکیبات آلی
شناسایی هالوژنها در ترکیبات آلی
آزمایش نیترات نقره
اگر در ساختمان ماده آلی نیتروژن یا گوگرد حضور داشته باشد با افزایش نیترات نقره به محلول اسیدی تهیه شده از ذوب قلیایی علاوه بر هالید نقره، رسوب سفید AgCN یا رسوب Ag2S نیز تشکیل میشود که مزاحم عمل تشخیص هالوژنها هستند
آزمایش نیترات نقره
اگر در ساختمان ماده آلی نیتروژن یا گوگرد حضور داشته باشد با افزایش نیترات نقره به محلول اسیدی تهیه شده از ذوب قلیایی علاوه بر هالید نقره، رسوب سفید AgCN یا رسوب Ag2S نیز تشکیل میشود که مزاحم عمل تشخیص هالوژنها هستند بنابراین قبل از رسوب دادن AgX باید گوگرد و نیتروژن را از محیط عمل خارج سازید، بدین طریق که به آن اسید نیتریک غلیظ افزوده و محلول حاصل را بجوشانید تا بر اثر تبخیر حجم آن به نصف تقلیل داده شود، سپس آنرا سرد کرده و با حجم مساوی آب مقطر رقیق کنید.سپس بر روی آن آزمایشات زیر را انجام دهید، اگر گوگرد و ازت وجود نداشته باشد نیازی به عمل فوق نیست.
الف) اگر در جسم آلی یک نوع هالوژن وجود داشته باشد حدود ۲ میلی لیتر از محلول زیر صافی حاصل از ذوب قلیایی را در یک لوله آزمایش بریزید و با اسید نیتریک رقیق آنرا اسیدی کرده مقداری محلول نیترات نقره اضافه کنید، رسوب تشکیل شده مشخص کننده نوع هالوژن خواهد بود، مایع رویی را بر اثر سرازیر کردن جدا کنید و به رسوب محلول رقیق آمونیاک اضافه نمائید اگر رسوب سفید بوده و به خوبی محلول در آمونیاک رقیق باشد نشانه کلر، و اگر زرد کمرنگ و به سختی محلول در آمونیاک باشد (کم محلول باشد) نشانه برم، اگر زرد پر رنگ و تقریبا نا محلول در آمونیاک باشد نشانه وجود ید در جسم آلی است.
ب) اگر مخلوط چند هالوژن وجود داشته باشد:
شناسایی ید
۲ میلی لیتر از محلول زیر صافی حاصل از ذوب قلیایی را در یک لوله آزمایش بریزید و با مقداری استیک اسید خالص (گلاسیال)، آنرا اسیدی کنید و سپس به آن حدود یک میلی لیتر تتراکلرید کربن بیفزائید و قطره قطره محلول نیتریت سدیم ضمن تکان دادن شدید لوله آزمایش اضافه کنید رنگ بنفش یا ارغوانی که در لایه آلی (CCl4) تشکیل میشود نشانه حضور ید است.
پس از تشخیص ید، از محلول همین لوله آزمایش برای تشخیص برم استفاده کنید. بدین طریق که مجددا مقداری محلول نیتریت سدیم افزوده و مقدار جزئی گرم کنید. بعد شدیدا تکان دهید و صبر کنید تا دو لایه از هم جدا شوند، لایه رویی را در لوله آزمایش تمیز دیگری بریزید و لایه بنفش رنگ تتراکلرید کربن را دور بریزید. به لایه رویی که در لوله آزمایش تمیز ریخته بودید یک میلی لیتر تترا کلرید کربن اضافه کنید و قطره قطره محلول ۲۰% نیتریت سدیم بیفزائید و در ضمن افزایش لوله را تکان دهید اگر باز هم لایه زیری رنگی شد محلول سدیم نیتریت بیشتری ریخته و پس از تکان دادن و سپس جدا شدن دو لایه، لایه رویی را به لوله آزمایش دیگری منتقل کنید و لایه زیری را دور بریزید و بر روی لایه رویی این عمل را آنقدر تکرار کنید تا دیگر لایه رنگی ایجاد نشود، در این صورت دیگر در محلول شما ید وجود ندارد. حال بر روی این محلول آزمایش تشخیص برم انجام دهید. (توجه کنید که اگر در ابتدای آزمایش رنگ بنفش ظاهر نشود نشانه عدم حضور ید در محلول است و بنابر این نیازی به استخراج ید نیست و از همان ابتدا میتوان برای تشخیص برم عمل کرد).
شناسایی برم
محلول اسیدی فوق را زیر هود حرارت دهید تا دیگر بخارات NO خارج نشود، سپس سرد کنید. محلول را با استیک اسید گلاسیال به شدت اسیدی کرده و مقدار کمی از دی اکسید سرب PbO2 اضافه نمائید. یک تکه کاغذ صافی آغشته به محلول فلورسئین را در بالای دهانه لوله آزمایش به دور دهانه چسبانده و حرارت دهید (کاغذ آغشته به فلورسئین به رنگ زرد لیمویی است) دی اکسید سرب در محلول استیک اسید تولید استات سرب میکند که HBr و HI را اکسید میکند ولی عملا تحت شرایط فوق بر HCl اثری ندارد.
(۱) ائوسین (قرمز رنگ) و (۲) فلوئورسئین (زردرنگ)
چون در داخل لوله آزمایش ید وجود ندارد اگر کاغذ آزمایش فلورسئین به رنگ صورتی در آید نشانه وجود برم در جسم آلی است (البته باید توجه داشت که ید نیز چنین جوابی میدهد بنابر این باید ابتدا ید را کاملا از محیط عمل خارج ساخت و سپس آزمایش مربوط به برم را انجام داد) برای تشخیص کلر از محتویات همین لوله استفاده میکنیم.
شناسایی کلر
اگر در آزمایش بالا کاغذ آزمایش فلورسئین به رنگ صورتی در نیاید دلیل آن است که در جسم مورد نظر برم شرکت ندارد در این صورت لوله آزمایش را با کمی آب مقطر بشوئید و محلول حاصل را صاف کنید و به محلول زیر صافی محلول رقیق اسید نیتریک و نیترات نقره اضافه کنید تشکیل رسوب سفید کلوئیدی نشانه وجود کلر است اما اگر در آزمایش قبل کاغذ آزمایش فلورسئین به رنگ صورتی در آید، عمل حرارت دادن را آنقدر ادامه دهید تا دیگر کاغذ آزمایش فلورسئین را به رنگ صورتی در نیاورد (در صورت لزوم مجددا کمی PbO و CH3COOH اضافه کنید) البته این آزمایش را میتوان بر محلول اولیه حاصل شده از ذوب قلیایی نیز انجام داد که در این صورت برم و ید هردو از محیط عمل خارج میشوند در این حالت حرارت را قطع کنید. پس از سرد شدن محلول محتویات آنرا با کمی آب مقطر بشوئید و صاف کنید و به محلول زیر صافی محلول رقیق اسید نیتریک و نیترات نقره اضافه کنید تشکیل رسوب سفید نشانه وجود کلر در جسم آلی است در اینجا برای انحلال این رسوب سفید نمیتوان از آمونیاک استفاده کرد، و اگر به محلول کلوئیدی فوق آمونیاک اضافه کنید مقدار رسوب سفید زیادتر خواهد شد. چرا؟ (یاد آوری: اگر ید و برم قبلا بطور کامل خارج نشده باشند، مقدار جزئی آنها نیز رسوب تقریبا سفید ایجاد خواهد کرد که با رسوب سفید کلرید نقره قابل اشتباه خواهد بود)
روش تشخیص هالوژنها با استفاده از آب کلر
اگر مخلوطی از هالوژنها داشته باشید برای تشخیص هر یک از آنها با آب کلر مطابق زیر عمل کنید:
مقدار ۲-۱ میلی لیتر از محلول زیر صافی حاصل از ذوب قلیایی را به وسیله اسید کلریدریک رقیق اسیدی کنید و یک میلی لیتر تتراکلرید کربن و سپس یک قطره آب کلر رقیق اضافه کنید (به وسیله اسیدی کردن محلول ۱۰% NaCl با ۲/۰ حجمش HCl رقیق محلول آب کلر تهیه کنید) این محلول را به شدت تکان دهید اگر ید وجود داشته باشد فاز تتراکلرید کربن (فاز زیری) برنگ ارغوانی در می آید اگر افزایش آب کلر ادامه یابد رنگ ارغوانی ابتدا شدید تر شده و سپس رو به کاهش می گذارد و بالاخره ناپدید میگردد (اکسید شدن ید رنگی به یدات بیرنگ).
اگر در این آزمایش برم وجود داشته باشد لایه زیری به رنگ قهوه ای یا قرمز ظاهر میشود که با افزایش کلر این رنگ ناپدید نخواهد گشت. بروش فوق نمیتوان کلر ار در جسم آلی تشخیص داد.
تهیه لاستیک سنتزی تیوکل (Tiokol)
تهیه لاستیک سنتزی تیوکل (Tiokol)
تیوکل ، لاستیکی سنتزی است که با افزودن گوگرد به انتهای زنجیرهایش ، استحکام و خواص ویژهای به خود میگیرد و خصلت ارتجاعی بیشتری پیدا میکند.
تیوکل ، پلیمری از اتیلن دیکلراید است که به آن ، گوگرد اضافه شده و فرمول نهایی بصورت C2H4S4 در آمده است. این ترکیب ، حدود ۸۲% گوگرد است و چون وزن مولکولی بالاست، ساختمانش احتمالا زنجیری است با گروه اتیلن مشخص و دست نخورده.

در تهیه این پلیمرها ، از هیدروکسیدسدیم استفاده میشود که با عمل جوشاندن تغلیظ میشود. این هیدروکسید غلیظ شده ، نصف گوگرد افزوده شده را جذب میکند و مادهای پودری شکل را بوجود میآورد. لذا هر چهار گروه اتم گوگرد دو به دو به طریقه متفاوتی از هم متصل شدهاند. مقدار در صد بالای گوگرد در ترکیب ، ناشی از سولفید سدیم تولیدی در اثر ترکیب هیدروکسید سدیم با گوگرد است.
اسیدی شدن محلول ، H2S و دیتیول اتیلن آزاد میکند. منشا تشکیل پلیمر ، پیوند دیسولفید در آن است:
SH2 + HS – CH2 – CH2 – SH
دو اتم گوگردی که توسط سدیم هیدروکسید جذب شده ، در پلیمر اولیه در محلول جامد نخواهد بود و توسط استن و جوشاندن قابل استخراج نیست. بعلاوه دو اتم گوگرد میتوانند با دو اتم گوگرد موجود در زنجیر کئوردینه شوند و بدین ترتیب قابل استخراج گردد. از طرفی چون مقادیر کمی از تتراسولفیدسدیم باقی میماند، احتمال تشکیل گروههای نهایی در مرکاپتان نیز میرود.
وسایل مورد نیاز:
- بشر
- بالن
- دستگاه رفلکس
- هیدروکسید سدیم
- پودر گوگرد
- دیکلرو اتان
هیدروکسید سدیم را در آب حل کرده ، میجوشانید تا تغلیظ شود. سپس به آن ، گوگرد اضافه کنید تا حدی که بیشتر گوگرد در آن حل گردد. بعد آن را در بالنی اضافه کرده و به آن دیکلرو اتان اضافه کنید و مخلوط را رفلکس کنید تا کلوئیدی اسفنجی تهی و تشکیل گردد.
نتیجه
یکی از خواص مهم پلی سولفیدها (که لاستیکی که تهیه کردهاید جزو آنهاست) ، مقاومت آنها در برابر حلال است. پلیمرها بر اساس خواص متفاوتشان کاربردهای زیادی پیدا میکنند. عده ای در تهیه و ساخت چسبها و رزینها و رنگها کاربرد دارند. عدهای دیگر فرم لاستیکی دارند و برای ساخت قطعاتی با حالت ارتجاعی بکار میروند.
لاستیک تیوکل در ساخت لولههای گاز اتومبیل و مراکز سرویس آنها ، پوششهای کابل ، پوشش منسوجات و بالن بسیار کاربرد دارد. از خواص مهم لاستیک تیوکل ، مقاومت فوقالعاده آنها در برابر حلال و روغن ، پایداری فوقالعاده در برابر کهنگی ، اوزون و نور آفتاب ونفوذ ناپذیری در برابر گازها و بخارهاست و بر اساس این خواص ، کاربرد وسیعی دارد.
تهیه لاستیک سنتزی تیوکل (Tiokol)
تهیه لاستیک سنتزی تیوکل (Tiokol)
تیوکل ، لاستیکی سنتزی است که با افزودن گوگرد به انتهای زنجیرهایش ، استحکام و خواص ویژهای به خود میگیرد و خصلت ارتجاعی بیشتری پیدا میکند.
تیوکل ، پلیمری از اتیلن دیکلراید است که به آن ، گوگرد اضافه شده و فرمول نهایی بصورت C2H4S4 در آمده است. این ترکیب ، حدود ۸۲% گوگرد است و چون وزن مولکولی بالاست، ساختمانش احتمالا زنجیری است با گروه اتیلن مشخص و دست نخورده.

در تهیه این پلیمرها ، از هیدروکسیدسدیم استفاده میشود که با عمل جوشاندن تغلیظ میشود. این هیدروکسید غلیظ شده ، نصف گوگرد افزوده شده را جذب میکند و مادهای پودری شکل را بوجود میآورد. لذا هر چهار گروه اتم گوگرد دو به دو به طریقه متفاوتی از هم متصل شدهاند. مقدار در صد بالای گوگرد در ترکیب ، ناشی از سولفید سدیم تولیدی در اثر ترکیب هیدروکسید سدیم با گوگرد است.
اسیدی شدن محلول ، H2S و دیتیول اتیلن آزاد میکند. منشا تشکیل پلیمر ، پیوند دیسولفید در آن است:
SH2 + HS – CH2 – CH2 – SH
دو اتم گوگردی که توسط سدیم هیدروکسید جذب شده ، در پلیمر اولیه در محلول جامد نخواهد بود و توسط استن و جوشاندن قابل استخراج نیست. بعلاوه دو اتم گوگرد میتوانند با دو اتم گوگرد موجود در زنجیر کئوردینه شوند و بدین ترتیب قابل استخراج گردد. از طرفی چون مقادیر کمی از تتراسولفیدسدیم باقی میماند، احتمال تشکیل گروههای نهایی در مرکاپتان نیز میرود.
وسایل مورد نیاز:
- بشر
- بالن
- دستگاه رفلکس
- هیدروکسید سدیم
- پودر گوگرد
- دیکلرو اتان
هیدروکسید سدیم را در آب حل کرده ، میجوشانید تا تغلیظ شود. سپس به آن ، گوگرد اضافه کنید تا حدی که بیشتر گوگرد در آن حل گردد. بعد آن را در بالنی اضافه کرده و به آن دیکلرو اتان اضافه کنید و مخلوط را رفلکس کنید تا کلوئیدی اسفنجی تهی و تشکیل گردد.
نتیجه
یکی از خواص مهم پلی سولفیدها (که لاستیکی که تهیه کردهاید جزو آنهاست) ، مقاومت آنها در برابر حلال است. پلیمرها بر اساس خواص متفاوتشان کاربردهای زیادی پیدا میکنند. عده ای در تهیه و ساخت چسبها و رزینها و رنگها کاربرد دارند. عدهای دیگر فرم لاستیکی دارند و برای ساخت قطعاتی با حالت ارتجاعی بکار میروند.
لاستیک تیوکل در ساخت لولههای گاز اتومبیل و مراکز سرویس آنها ، پوششهای کابل ، پوشش منسوجات و بالن بسیار کاربرد دارد. از خواص مهم لاستیک تیوکل ، مقاومت فوقالعاده آنها در برابر حلال و روغن ، پایداری فوقالعاده در برابر کهنگی ، اوزون و نور آفتاب ونفوذ ناپذیری در برابر گازها و بخارهاست و بر اساس این خواص ، کاربرد وسیعی دارد.
توجیه پدیده کف
توجیه پدیده کف :
فعال کننده های سطحی با توجه به نوع گروه قطبی موجود در آن ها طبقه بندی می شوند یکی از آنها فعال کننده های سطحی آنیونی هستند. این مولکول ها معمولا نمک های سولفونات و سولفات اسید های چرب با طول زنجیر از ۸ تا ۱۲ اتم کربن هستند که در تهیه مواد شوینده به کار می روند. سدیم دو دسیل سولفونات از مهمترین و پر کاربرد ترین عوامل فعال سطحی آنیونی هستند.
اگر این مولکولها در محلول آبی قرار گیرند دم هیدروکربنی آنها توسط مولکول های آب دفع شده و در یک اجتماع ۳۰ تا ۳۰۰ مونومری به طریقی کنار هم جمع می شوند که قسمت های آبگریز مولکول کنار هم قرار گرفته و از تماس با توده محلول قطبی محافظت می شوند به چنین اجتماعی مایسل گفته می شود.
مایسل ها کره های با سطح قطبی و مرکز غیر قطبی ,محلی مناسب برای انحلال مولکول های غیر قطبی شامل چربی ها و لک های گرد وغبار و کثافت, هستند. بنابراین به نظر میرسد یک امولوسیون از قطره های روغن پخش شده در آب ایجاد شده است که این پایداری مدیون حضور ملکول ها ی فعال کننده سطح به صورت مایسل است.

برای توجیه پدیده کف می توان گفت:
با تکان دادن محلول آب و صابون حباب های ریز هوا در محلول آب و صابون گیر می افتند و یک سطح جدید گاز مایع تشکیل می شود. تشکیل سطح باافزایش کشش سطحی همراه است. حضور مولکول های فعال کننده سطحی در توده محلول کشش سطحی را کاهش میدهد پس یک گرادیانت کشش سطحی بین محلول و سطح جدید ایجاد می شود و باعث حرکت مولکول های فعال سطحی از توده محلول به سطح جدید و حرکت مخالف حلال (آب)از سطح به توده محلول می شود در نتیجه سطح ایجاد شده بدون آب شده و پایدارمی شود و به مرور افزایش می یابد بنابراین حباب ها بزرگتر شده و کف ایجاد می شود.
توجیه پدیده کف
توجیه پدیده کف :
فعال کننده های سطحی با توجه به نوع گروه قطبی موجود در آن ها طبقه بندی می شوند یکی از آنها فعال کننده های سطحی آنیونی هستند. این مولکول ها معمولا نمک های سولفونات و سولفات اسید های چرب با طول زنجیر از ۸ تا ۱۲ اتم کربن هستند که در تهیه مواد شوینده به کار می روند. سدیم دو دسیل سولفونات از مهمترین و پر کاربرد ترین عوامل فعال سطحی آنیونی هستند.
اگر این مولکولها در محلول آبی قرار گیرند دم هیدروکربنی آنها توسط مولکول های آب دفع شده و در یک اجتماع ۳۰ تا ۳۰۰ مونومری به طریقی کنار هم جمع می شوند که قسمت های آبگریز مولکول کنار هم قرار گرفته و از تماس با توده محلول قطبی محافظت می شوند به چنین اجتماعی مایسل گفته می شود.
مایسل ها کره های با سطح قطبی و مرکز غیر قطبی ,محلی مناسب برای انحلال مولکول های غیر قطبی شامل چربی ها و لک های گرد وغبار و کثافت, هستند. بنابراین به نظر میرسد یک امولوسیون از قطره های روغن پخش شده در آب ایجاد شده است که این پایداری مدیون حضور ملکول ها ی فعال کننده سطح به صورت مایسل است.

برای توجیه پدیده کف می توان گفت:
با تکان دادن محلول آب و صابون حباب های ریز هوا در محلول آب و صابون گیر می افتند و یک سطح جدید گاز مایع تشکیل می شود. تشکیل سطح باافزایش کشش سطحی همراه است. حضور مولکول های فعال کننده سطحی در توده محلول کشش سطحی را کاهش میدهد پس یک گرادیانت کشش سطحی بین محلول و سطح جدید ایجاد می شود و باعث حرکت مولکول های فعال سطحی از توده محلول به سطح جدید و حرکت مخالف حلال (آب)از سطح به توده محلول می شود در نتیجه سطح ایجاد شده بدون آب شده و پایدارمی شود و به مرور افزایش می یابد بنابراین حباب ها بزرگتر شده و کف ایجاد می شود.
توجیه پدیده کف
توجیه پدیده کف :
فعال کننده های سطحی با توجه به نوع گروه قطبی موجود در آن ها طبقه بندی می شوند یکی از آنها فعال کننده های سطحی آنیونی هستند. این مولکول ها معمولا نمک های سولفونات و سولفات اسید های چرب با طول زنجیر از ۸ تا ۱۲ اتم کربن هستند که در تهیه مواد شوینده به کار می روند. سدیم دو دسیل سولفونات از مهمترین و پر کاربرد ترین عوامل فعال سطحی آنیونی هستند.
اگر این مولکولها در محلول آبی قرار گیرند دم هیدروکربنی آنها توسط مولکول های آب دفع شده و در یک اجتماع ۳۰ تا ۳۰۰ مونومری به طریقی کنار هم جمع می شوند که قسمت های آبگریز مولکول کنار هم قرار گرفته و از تماس با توده محلول قطبی محافظت می شوند به چنین اجتماعی مایسل گفته می شود.
مایسل ها کره های با سطح قطبی و مرکز غیر قطبی ,محلی مناسب برای انحلال مولکول های غیر قطبی شامل چربی ها و لک های گرد وغبار و کثافت, هستند. بنابراین به نظر میرسد یک امولوسیون از قطره های روغن پخش شده در آب ایجاد شده است که این پایداری مدیون حضور ملکول ها ی فعال کننده سطح به صورت مایسل است.

برای توجیه پدیده کف می توان گفت:
با تکان دادن محلول آب و صابون حباب های ریز هوا در محلول آب و صابون گیر می افتند و یک سطح جدید گاز مایع تشکیل می شود. تشکیل سطح باافزایش کشش سطحی همراه است. حضور مولکول های فعال کننده سطحی در توده محلول کشش سطحی را کاهش میدهد پس یک گرادیانت کشش سطحی بین محلول و سطح جدید ایجاد می شود و باعث حرکت مولکول های فعال سطحی از توده محلول به سطح جدید و حرکت مخالف حلال (آب)از سطح به توده محلول می شود در نتیجه سطح ایجاد شده بدون آب شده و پایدارمی شود و به مرور افزایش می یابد بنابراین حباب ها بزرگتر شده و کف ایجاد می شود.
ترکیبات آلی شامپو
ترکیبات آلی شامپو
شامپو از دو قسمت عمده تشکیل شده است:
۱- مواد فعال سطحی: جزء اصلی یک شامپو مواد فعال کننده سطحی آن است.
موادفعال کننده سطح به طورکلی به چهار دسته آنیونی، کاتیونی، آمفوتری و غیر یونی تقسیم بندی می شوند. در شامپو معمولا ترکیبی از مواد فعال آنیونی (مانند سدیم لارت سولفات)، مواد آمفوتری (مانند بتائین ها) و مواد غیریونی (مانند کوکونات فتی اسید دی اتانول آمید) به عنوان مواد فعال کننده سطحی یا جزء اصلی استفاده می شود.
۲- افزودنی ها: بفیه اجزاء به عنوان افزودنی به شامپو اضافه می شوند…

افزودنی های شامپو خود به دو دسته تقسیم بندی می شوند:
الف- افزودنی های عمومی
موادی مانند نگهدارنده ها برای جلوگیری از آلودگی میکروبی، نمک برای افزایش قوام شامپو و اسانس برای خوشبو نمودن شامپو و ا.د.ت.آ (EDTA) برای کاهش سختی آب و سیتریک اسید جهت تنظیم پ هاش جزء افزودنی های شامپو به حساب می آیند. اگر به ترکیبات تشکیل دهنده شامپوهادقت کنیم خواهیم دید اجزائی مثل اسیدسیتریک، نمک، ا.د.ت.ا، نگهدارنده، اسانس، رنگ و آب در همه شامپوها مشترک هستند بنابراین در انتخاب شامپو دقت به این موارد اهمیتی ندارد.
ب- افزودنی های اختصاصی
در فرمولاسیون شامپوهای نوین مواد ویژه ای برای خلق اثربخشی خاص به شامپو اضافه می گردند تا شامپو علاوه بر شویندگی بتواند ویژگی های زیبایی مورد انتظار را نیز برآورده نماید. در انتخاب شامپوی مناسب دقت به مواد فعال کننده سطح و همچنین افزودنی های اختصاصی بسیار مهم است.
در برخی از شامپوهای جدید اجزاء ویژه ای به نام ضخیم کننده(Thickner) اضافه شده است. این شامپوها در واقع سطح تارهای مو را با لایه ای از پروتئین می پوشانند بنابراین باعث می شوند هربار که شما این شامپو را استفاده می کنید موی شما پر پشت تر به نظر برسد.
پروتئین کراتین و آمینو اسیدها به ساقه مو می پیوندند و شکافهای ایجاد شده در اثر استفاده از مواد نامرغوب را پر می کند. این امر باعث افزایش مقاومت مو و محافظت از آن می گردد. پروتئین تخم مرغ با مو پیوند ایجاد نمی کند بنابراین استفاده از آن در شامپو فقط یک مانور تبلیغاتی (Gimmick) است.
مواد مرطوب کننده، موی شما را هیدراته می کند درست همان اثری که بر روی پوست هم دارد.
پنتنول و ویتامین ب۵ برخلاف بقیه ویتامین ها به داخل محور مو نفوذ می کنند و برای افزایش استحکام و سلامت مو مفید می باشد. (دقت کنید که از ویتامین برای افزودن خواص نرم کنندگی استفاده شده نه تغذیه و تقویت مو)
هرچند پروتئین موجود در شامپو ها به داخل محور مو نفوذ نمی کنند اما با پوشانیدن سطح مو باعث پرپشت به نظر آمدن و افزایش خاصیت نرم کنندگی می شوند.
پروتئین ابریشم به افزایش درخشندگی مو کمک می کند.
سال نو مبارک
سال 1394 مبارک باد.

کاش وقتی زندگی فرصت دهد
گاهی از پروانه ها یادی کنیم
کاش بخشی از زمان خویش را
وقف قسمت کردن شادی کنیم
کاش وقتی آسمان بارانی ست
از زلال چشم هایش تر شویم
وقت پاییز از هجوم دست باد
کاش مثل پونه ها پر پر شویم
کاش وقتی چشم هایی ابریند
به خود اییم و سپس کاری کنیم
از نگاه زرد گلدان هایمان
کاش با رغبت پرستاری کنیم
کاش دلتنگ شقایق ها شویم
به نگاه سرخ شان عادت کنیم
کاش شب وقتی که تنها می شویم
با خدای یاس ها خلوت کنیم
تهیه ی شناساگر در آزمایشگاه شیمی

1 - تهیه آب آهک
۵گرم اکسید کلسیم رادر۱۵۰میلی لیتر آب حل کنید. این محلول کدر، شیرآهک نامیده می شود. شیر آهک را با کاغذ صافی، صاف کنید. محلول صاف شده کاملا شفاف، آب آهک است.
۱- تهیه آب آهک
۵گرم اکسید کلسیم رادر۱۵۰میلی لیتر آب حل کنید. این محلول کدر، شیرآهک نامیده می شود. شیر آهک را با کاغذ صافی، صاف کنید. محلول صاف شده کاملا شفاف، آب آهک است۰
۲- تهیه محلول لوگل
برای تست نشاسته، بی حرکت کردن تاژکداران و مشخص کردن هسته یک گرم یدورپتاسیم را با ۲۵/۰ گرم ید جامد مخلوط کرده و در۱۰۰سی سی الکل صنعتی حل می کنیم.
۳-تهیه محلول ید
برای رنگ آمیزی سلول های پوششی دهان و تست نشاسته ۲۵/۰ گرم ید جامد را در ۱۰۰سی سی الکل صنعتی حل می کنیم
۴-تهیه محلول تورنسل
معرف اسیدهاو بازها
یک گرم تورنسل را در کمی آب مقطر حل کرده و حجم آنرا به ۱۰۰سی سی می رسانیم.
۵-تهیه محلول هلیانتین(متیل اورانژ)
معرف اسید و بازها
یک دهم گرم آن را در۱۰۰سی سی آب مقطرحل می کنیم.
۶-تهیه محلول فنل فتالئین
۲گرم پودر فنل فتالئین رادر۵۰سی سی الکل حل کرده با آب مقطر به۱۰۰سی سی می رسانیم.
۷-تهیه محلول نیترات نقره
برای شناخت نمک درعرق- آب معمولی و…
یک گرم پودر نیترات نقره را در۱۰۰سی سی آب مقطرحل می کنیم و در شیشه های تیره نگهداری مس کنیم.
۸-تهیه محلول گیمسا
برای رنگ آمیزی گلبول های سفید
یک گرم پودر گیمسا را با ۶۰ سی سی گلیسیرین مخلوط نموده و به مدت ۱ساعت در گرم خانه ۶۰ درجه گرما نگهداری می کنیم. پس از خروج ۶۶ سی سی الکل متیلیک ۹۷درجه به به آن اضافه می کنیم. این محلول به نام محلول ذخیره گیمسا است . به هنگام استفاده ۵/۲سی سی از این محلول را با ۳سی سی الکل متیلیک مخلوط کرده و ۱۰۰ سی سی آب مقطر به آن اضافه می کنیم.
۹- تهیه محلول فوشین قلیایی
برای رنگ آمیزی بافت های سلولزی در مدت ۵ ثانیه
یک گرم فوشین قلیایی را در۱۰۰سی سی الکل۹۵ درجه حل کرده و ۱۰۰سی سی آب مقطر به آن اضافه می کنیم.
۱۰- تهیه محلول کارمن زاجی
برای رنگ آمیزی بافت های سلولزی در مدت ۱۵دقیقه
برای رنگ کردن بافت های سلولزی به مدت ۲-۱دقیقه در یک بشر به حد اشباع زاج پتاس در آب حل می کنیم و بوسیله چراغ الکلی آن را به جوش می آوریم سپس یک گرم کارمن قرمز را در هاون سایئده به زاج در حال جوش اضافه می کنیم.۱۰دقیقه بجوشد و پس از سرد شدن آن را با کاغذ صافی، صاف کرده و چند قطره اسید فنیک (برای جلوگیری از فساد) به آن اضافه می کنیم.
۱۱- تهیه چسب نشاسته
یک گرم نشاسته را در ۱۰۰سی سی آب مقطر ریخته و بهم می زنیم. سپس تا نقطه جوش حرارت داده و توسط کاغذ صافی، صاف می کنیم.
۱۲- تهیه آب ژاول
برای از بین بردن ترکیبات داخل سلول
در یک شیشه مقداری پر منگنات پتاسیم ریخته و دهانه شیشه را به وسیله چوب پنبه دو سوراخه می بندیم .از یکی از سوراخ های آن بوسیله بورت شیر دار که در آن اسید کلرید ریک ریخته ایم اسید به پر منگنات اضافه می کنیم. از سوراخ دیگر چوپ پنبه لوله خمیده ای عبور می دهیم که سر دیگر آن در داخل سود سوز آور در داخل یک ارلن وارد شود. اسید با پر منگنات کلر آزاد کرده است و کلر با سود سوز آور ترکیب شده و هیپو کلرید سدیم می دهد
۱۳٫ تهیه محلول سولفات مس
برای شناخت پروتئین
یک گرم سولفات مس (کات کبود) را در cc 100 آب مقطر حل می کنیم .
۱۴٫ تهیه سولفات مس بدون آب
حدود ۵ گرم سولفات مس آبی رنگ را در یک لوله آزمایش ریخته و روی شعله آنقدر حرارت می دهیم تا پودر آبی رنگ سفید شود .
۱۵٫تهیه محلول سود ۱۰%
برای تست پروتئین
۱۰ گرم سود جامد را با ترازو وزن کرده سپس آنرا در۱۰۰ آب مقطر حل کرده و خوب بهم می زنیم .
۱۶ . تهیه محلول پتاس ۵%
co2 برای جذب
۲۰ گرم پتاس جامد را وزن کرده و آن را در ۴۰۰ سی سی آب حل می کنیم.
۱۷- تهیه اسید کلریدریک ۵/۰ نرمال
۵۰۰سی سی آب مقطر را با ۵/۲۱ سی سی اسید کلرید ریک تجاری مخلوط می کنیم.
۱۸- تهیه اسید کلریدریک ۱ نرمال
۱۰۰سی سی اب مقطر را با۱/۸ سی سی اسید کلرید ریک تجاری مخلوط می کنیم.
۱۹- تهیه محلول بیکربنات پتاسیم
برای دفع Co2
۵ گرم بیکربنات پتاسیم را در ۱۰۰سی سی آب مقطر حل می کنیم.
۲۰- تهیه آبی تولوئیدین
برای رنگ آمیزی کرو موزوم ها
نیم گرم پودر آن را در۱۰۰سی سی آب مقطر حل می کنیم.
۲۱- تهیه استو کار من
برای رنگ آمیزی کروموزم ها
یک گرم کارمن را در ۵۵ سی سی آب مقطرمی جوشانیم.
۲۲- تهیه برم تیمول بلو
یک گرم پودر برم تیمول را در یک لیتر آب مقطر حل کرده و یک یا دو قطره آمونیک به آن اضافه می کنیم.
۲۳- تهیه بلودومتیل
نیم گرم پودر تجاری بلودومتیل را در یک لیتر آب مقطر حل می کنیم.
۲۴- تهیه سبز ید
برای رنگ آمیزی بافت های سلولزی در۳۰ ثانیه
یک گرم سبز ید را در۱۰۰سی سی الکل ۷۰ درجه حل می کنیم.
۲۵- تهیه محلول گلوکز%۱
یک گرم گلوکز را به مقداری آب اضافه کرده و حجم آن را به۱۰۰ سی سی می رسانیم.
۲۶- تهیه کشت مخمر
یک گرم پودر گلوکز را در ۱۰۰ سی سی آب حل کرده یک قاشق چایخوری خمیرترش نان به آن اضافه کنید و هم بزنید.این ظرف را به مدت یک ساعت در حرارت۳۷درجه قراردهید.
۲۷- تهیه کشت پارامسی
مقداری یونجه را درظرفی خیس کرده(بهتر است یونجه ها رادریک تا دو هفته قبل از آزمایش خیس کرد و در حرارت هوای آزمایشگاه قرارداد.)
۲۸- تهیه محلول پپسین
۶ گرم پودر پپسین رادر۱۵۰سی سی آب درون یک بشر کوچک حل می کنیم.
۲۹- تهیه معرف بیوره
۴ گرم سود را در۵۰۰ سی سی آب مقطر حل می کنیم سپس۳ گرم سولفات مس آبدار به آن اضافه کرده پس از افزودن ۵ گرم یدور پتاسیم به محلول ۹گرم تارتارات مضاعف سدیم و پتاسیم اضافه کرده و خوب هم زده محلول حاصله آبی رنگ است.در صورت ظاهر شدن رسوب سیاه یاقرمز محلول،خراب است.
۳۰- تهیه محلول قرمز کنگو
برای رنگ کردن بافت های سلولزی
یک گرم پودر آن را در ۱۰۰سی سی آب مقطر حل می کنیم.
۳۱- تهیه قرمز خنثی
برای مشاهده واکوئل های درپارامسی
یک گرم پودر آن را با ۱۰۰ سی سی آب مقطر مخلوط کرده و به هم زده تا محلول یک در صد بوجود بیاید .
۳۲- تهیه محلول فیکساتور
برای نگهداری بافت های گیاهی در ان مقدار ۱۵۰ سی سی الکل ۹۰ درجه را با مقدار ۱۰۰ سی سی فرمل ۵% مخلوط کرده بعد مقدار ۵۰ سی سی گلیسیرین به آن می افزاییم .
۳۳- تهیه محلول سبز متیل
برای رنگ کردن بافت های چوبی گیاهان در مدت ۳۰ ثانیه
یک گرم پودر تجارتی را در ۱۰ سی سی الکل ۷۰ درجه حل کرده و با آب مقطر حجم آن را به ۱۰۰ سی سی میرسانیم .
۳۴- تهیه محلول بندکیت کیفی
۱۷۳ گرم سیترات سدیم و ۱۰۰ گرم کربنانت سدیم بی اب را در۸۰۰ سی سی آب مقطر به کمک گرما حل می کنیم . در ظرف دیگری ۳/۱۷ گرم سولفات مس متبلور در ۱۰۰ سی سی آب مقطر حل کرده به تدریح به محلول سیترات کربنات اضافه می کنیم و حجم محلول را به یک لیتر می رسانیم.
۳۵- تهیه فهلینک
برای شناخت گلو کز
۳۴ گرم سولفاد مس متبلور را در مقدار کمی اب مقطر به کمک حرارت حل کرده و حجم ان را به۵۰۰ سی سی می رسا نیم.
۳۶- تهیه فهلینگ
برای شناخت گلوکز
۱۷۳ گرم تارتارات سدیم و پتاسیم را (نمک راشل) در کمی آب حل کرده و ۱۰۰سی سی سود ۱۵% بدان می افزائیم و حجم محلول را به ۵۰۰ سی سی می رسانیم.
۳۷- تهیه محلول بیسمارک
یک گرم پودر قهوه ای بیسمارک را در۱۰۰سی سی الکل ۸۰ درجه حل می کنیم.
۳۸- تهیه اسید کلریدریک رقیق
اسید کلریدریک ۳۷% را توسط یک استوانه مدرج برداشته داخل بشر حاوی ۱۵۰ سی سی آب مقطر می ریزیم . این اسید برای آزمایش هضم پروتئین می باشد .
۳۹- تهیه محلول جهت شمارش گلبول های قرمز
۱/. گرم نمک طعام ، ۵/۳ گرم سولفات سدیم ، ۲۵/. گرم کلرور جیوه ، حجم آنها را با آب مقطر به ۱۰۰ سی سی می رسانیم .
۴۰- محلول ۳۰% کلرور کبالت
برای مشاهده اثر روزنه ها
۳۰ گرم بلور کلرور کبالت را با ۱۰۰ سی سی آب مقطر پس از حل کردن آن را صاف می کنیم .
۴۱- تهیه سود رقیق
برای هضم پروتئین ها
۴ گرم سود را در مقداری آب حل کرده و حجم آن را به یک لیتر می رسانیم .
۴۲- تهیه معرف تالن (محلول نیترات نقره آمونیاکی)
به ۳ سی سی محلول نیترات نقره ۳ قطره محلول سود اضافه کنید . رسوب قهوه ای رنگ Hg2o تولید می شود .سپس محلول آمونیاک به آن بیافزایید تا رسوب حل شود .
۴۳- تهیه معرف شیف
۱/. گرم فوشین در ۱۰۰ سی سی آب مقطر به این محلول گاز so2 سولفیت سدیم و کمی Hcl اضافه می کنیم .
۴۴- تهیه محلول لوکاس
برای تشخیص انواع الکل ها
۱۷گرم کلرید روی بدون آب مذاب شده را در ۵/۱۱ میلی لیتر محلول Hcl ۳۷% حل کرده و به هم زده و بعد در دسیکاتور خشک شده و دیگر بخارات اسید از آن بلند نشود استفاده می کنیم.
فرمول های تولید شامپو
فرمول های تولید شامپو
کرم شامپو، انواع شامپو از نوع سفت تا نرم را در بر می گیرد. این شامپوها را میتوان از مخلوطی از سدیم لوریل سولفات و صابون که شامپو را غلیظ تر می کند تهیه نمود.

فرمول شماره یک
خمیر سدیم لوریل سولفات ۲۵ گرم لانولین ۲۵/۰ گرم
ستیل الکل ۵/۰ گرم اسانس معطر چند قطره
اسید استاریک ۵/۶ گرم سود کاستیک ۱ گرم
آب مقطر ۶۸ میلی لیتر ماده محافظ و ماده رنگی به مقدار لازم
۱- اسید استاریک، سدیم لوریل سولفات و لانولین را حرارت دهید و ۸۰ درصد آب را تا ۸۰ درجه سانتیگراد جداگانه حرارت دهید.
۲- هر دو قسمت را بر هم افزوده و خوب بهم بزنید تا مخلوط یکنواختی حاصل شود.
۳- سود سوزآور و باقیمانده آب را حرارت دهید تا کاملاً حل شود.
۴- محلول سود را با سایر مواد آماده شده مخلوط کنید و برای مدت ۱۵ دقیقه بهم بزنید. هنگامی که مخلوط تا ۴۰ درجه حرارت سرد شد اسانس و رنگ و ماده محافظ را اضافه کنید و مجدداً بهم بزنید.
فرمول شماره دو
مانو کول Manucol SS/LH (آلژینات سدیم) ۱۶ گرم
خمیر سدیم لوریل سولفات ۳۰ گرم کلرید سدیم ۴ گرم
آب مقطر ۵۰ میلی لیتر عطر ۳-۱ قطره
ماده محافظ ( نیپاژین M) خیلی کم
۱- تمام مواد مورد نیاز را به دقت وزن نمایید.
۲- در یک ظرف مانوکول را در آب حل نمایید.
۳- در یک هاون کلرید سدیم را با خمیر لوریل سولفات مخلوط نمایید.
۴- محلول آبی را تا حدود ۷۰ درجه حرارت دهید.
۵- مخلوط کلرید سدیم و خمیر لوریل سولفات را به آب اضافه کرده و بهم بزنید. صبر کنید تاخنک شود. عطر، رنگ و ماده محافظ را اضافه کنید.
توجه : برای حل کردن مانوکول در آب، ابتدا مقدار کمی آب اضافه نموده و بهم بزنید تا یک خمیر تهیه شود، سپس بقیه آب را اضافه نمایید، بهتر است ابتدا پودر مانوکول را بامقار کمی گلیسیرین یا الکل ساییده، سپس آب را اضافه نمایید. از آب داغ استفاده نکنید زیرا چسبندگی امولسیون را از بین می برد.
مانوکول به عنوان ماده غلیظ کننده به کار می رود.
فرمول شماره سه
خمیر سدیم لوریل سولفات ۲۵ گرم دی اتیلن گلیکول منو استئارات ۲ گرم
آب مقطر ۶۷ میلی لیتر رنگ خیلی کم
هیدروکسید سدیم ۷۵/۰ گرم اسید استئاریک ۵ گرم
عطر ۳-۱ قطره ماده محافظ ( نیپاژین M) خیلی کم
۱- هیدروکسید سدیم را در آب حل نموده تا ۷۰ درجه سانتیگراد حرارت دهید.
۲- به استثنای ماده رنگی و عطر بقیه مواد را تا دمای ۷۰ درجه سانتیگراد حرارت دهید، سپس به محلول هیدروکسید سدیم اضافه نمایید.
۳- مخلوط را تا خنک شدن بهم بزنید.
۴- عطر و ماده رنگی را بعد از خنک شدن امولسیون و رسیدن حرارت آن به ۴۵ درجه سانتیگراد اضافه نمایید.
فرمول شماره چهار
خمیر سدیم لوریل سولفات ۲۵ گرم هیدروکسید سدیم جامد ۱ گرم
ماده محافظ ( نیپاژین M) خیلی کم اسید استئاریک ۷ گرم
آب مقطر ۶۷ میلی گرم عطر ۳-۱ قطره
۱- خمیر سدیم لوریل سولفات، اسید استئاریک و نصف مقدار آب را حرارت دهید تا یک مایع صاف کاملاً یکنواخت بدون ذرات ذوب نشده به دست آید( ۷۰ درجه سانتیگراد).
۲- هیدروکسید سدیم و ماده محافظ را در بقیه آب در حرارت ۷۰ درجه سانتیگراد حل نمایید.
۳- محلول شماره دو را به محلول شماره یک اضافه نموده و پیوسته بهم بزنید تا مخلوط یکنواختی به دست آید، سپس بگذارید تا خنک شود. هنگامی که درجه حرارت به ۳۵ رسید عطر را به آن اضافه کنید.
فرمول شماره پنج
خمیر سدیم لوریل سولفات ۵۰ گرم هیدروکسید سدیم ۱ گرم
عطر ۳-۱ قطره اسید استئاریک ۷ گرم
ماده محافظ ( نیپاژین M) خیلی کم آب مقطر ۴۲ میلی لیتر
همانند فرمول شماره چهار تهیه شود.
فرمول شماره شش
الف : خمیر سدیم لوریل
سولفات ۵۰ گرم ایزوپروپانول آمید ۳ گرم
اسید استئاریک ۷ گرم
ب: سدیم هیدروکسید ۱ گرم
آب مقطر ۴۰ میلی لیتر ماده محافظ ( نیپاژین M) خیلی کم
عطر ۳-۱ قطره
مواد بخش «الف» را حرارت دهید( تا ۷۰ درجه سانتیگراد) مواد بخش «ب» را تا ۷۰ درجه سانتیگراد حرارت دهید. مخلوط «ب» را به مخلوط «الف» اضافه نموده و تا به دست آمدن یک امولسیون بهم بزنید. عطر را در حرارت ۳۵ درجه اضافه نمایید.
فرمول شماره هفت (کرم شامپوی مایع)
خمیر سدیم لوریل سولفات ۲۵ گرم استئارات منیزیم ۲ گرم
مانوکول SS/44 خیلی کم عطر ۳-۱ قطره
پلی اتیلن گلیکول منو استئارات ۵ گرم الکل الئیل ۳-۱ قطره
آب مقطر ۶۸ میلی لیتر ماده محافظ ( نیپاژین M) خیلی کم
۱- استئارات منیزیم را با خمیر سدیم لوریل سولفات مخلوط نمایید.
۲- پلی اتیلن گلیکول منو استئارات را به آب اضافه کنید و بهم بزنید، سپس الکل الئیل را به آن اضافه کنید. مخلوط را تا ۷۵ درجه سانتیگراد حرارت دهید.
۳- با بهم زدن دائم بقیه آب را به مخلوط اضافه کنید.
۴- عطر، ماده محافظ و سایر مواد را در ۴۰ درجه سانتیگراد اضافه نمایید.
فرمول شماره هشت «کرم ضد شوره»
خمیر سدیم لوریل سولفات ۲۵ گرم آب مقطر ۶۵ میلی لیتر
آب مقطر ۶۵ میلی لیتر اسید استئاریک ۷ گرم
پودر بیوسولفور ۲ گرم ماده محافظ ( نیپاژین M) خیلی کم
عطر ۱ قطره
هیدروکسید سدیم را در آب با حرارت ۷۵ درجه سانتیگراد حل نمایید.
به محلول هیدروکسید سدیم بیوسولفور را اضافه کنید. اسید استئاریک و خیمر سدیم لوریل سولفات را مخلوط نموده و تا حرارت ۶۰ درجه به آرامی گرم نمایید، سپس حاصل را به محلول آبی اضافه کنید و تا خنک شدن بهم بزنید و در پاین ماده محافظ و عطر را به آن بیفزایید.









